题目内容
【题目】如图所示电池是一种新型储氢材料—镍电池(MHn—Ni),(MHn中金属和氢都为 0 价)。下列有关说法不正确的是
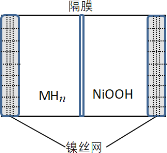
A.放电时正极反应为 NiOOH+H2O+e-→Ni(OH)2+OH-
B.电池的电解液可为KOH 溶液
C.充电时阴极反应为 MHn+nOH--e-→nH2O+M
D.MHn 是一类储氢材料,n 越大,电池的比能量越高
【答案】C
【解析】
根据图示,镍电池(MHn—Ni)中应该选碱性溶液作电解质溶液,放电时,正极:NiOOH+H2O+e-=Ni(OH)2+OH-,负极:MHn+nOH--ne-=M+nH2O,总反应:MHn+nNiOOH=M+nNi(OH)2 ,充电时,阳极反应:Ni(OH)2+OH--e-=NiOOH+H2O,阴极反应:M+nH2O+ne-=MHn+nOH-,总反应:M+nNi(OH)2=MHn+nNiOOH;据此分析解答。
A.放电时,正极发生还原反应:NiOOH+H2O+e-=Ni(OH)2+OH-,故A正确;
B.为了防止MHn被氢离子氧化,镍电池中电解液应该为碱性溶液,可以用KOH作电解液,故B正确;
C.充电时,电池的负极作阴极,阴极发生还原反应:M+nH2O+ne-=MHn+nOH-,故C错误;
D.M为储氢合金,MHn为吸附了氢原子的储氢材料,其氢密度越大,电池的能量密度越高,故D正确;
故选C。

 字词句段篇系列答案
字词句段篇系列答案【题目】以天然气代替石油生产液体燃料和基础化学品是当前化学研究和发展的重点。
(1)我国科学家创造性地构建了硅化物晶格限域的单中心铁催化剂,成功实现了甲烷一步高效生产乙烯、芳香烃Y和芳香烃Z等重要化工原料,实现了CO2的零排放,碳原子利用率达100%。已知Y、Z的相对分子质量分别为78、128,其一氯代物分别有1种和2种。
①有关化学键键能数据如表中所示:
化学键 | H-H | C=C | C-C | C≡C | C-H |
E(kJ/mol) | 436 | 615 | 347.7 | 812 | 413.4 |
写出甲烷一步生成乙烯的热化学方程式:_____________;
②已知:原子利用率=期望产物总质量/反应物总质量×100%,则甲烷生成芳香烃Y的原子利用率为______;
③生成1 mol Z产生的H2约合标准状况下________L。
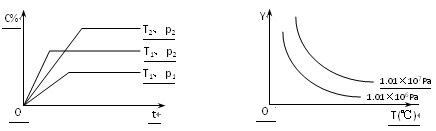
(2)如图为乙烯气相直接水合法制备乙醇过程中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
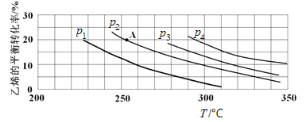
①若p2=8.0 MPa,列式计算A点的平衡常数Kp=_______(用平衡分压代替平衡浓度计算;分压=总压×物质的量分数;结果保留到小数点后两位);
②该反应为______(填“吸热”或“放热”)反应,图中压强(p1、p2、p3、p4)的大小关系为_______;