题目内容
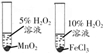
1. ClO2 是一种高效安全的杀菌消毒剂.用氯化钠电解法生成ClO2的工艺原理示意图如图,发生器内电解生成ClO2.下列说法正确的是( )
ClO2 是一种高效安全的杀菌消毒剂.用氯化钠电解法生成ClO2的工艺原理示意图如图,发生器内电解生成ClO2.下列说法正确的是( )| A. | a气体是氯气,b气体是氢气 | |
| B. | 氯化钠电解槽内每生成2 mol a气体,转移2mol e- | |
| C. | ClO2发生器中阴极的电极反应式为:2ClO3-+12H++10e-═Cl2↑+6H2O | |
| D. | 为使a、b气体恰好完全反应,理论上每生产1molClO2需要补充56L(标准状况)b气体 |
分析 根据流程图可知道:食盐水在特定条件下电解得到氯酸钠(NaClO3)、氢气,NaClO3和HCl反应,生成ClO2、氯气和氯化钠,b气体为氯气,a气体为氢气,
A.a为氢气,b为氯气;
B.电解食盐水得到氯酸钠(NaClO3)和H2,电解的离子反应方程式为:Cl-+3H2O$\frac{\underline{\;通电\;}}{\;}$ClO3-+3H2↑;
C.ClO2发生器中的反应为,化学方程式NaClO3和盐酸发生歧化反应,生成NaCl、ClO2、Cl2、H2O,阴极是ClO3-得到电子生成ClO2;
D.NaClO3和盐酸发生歧化反应,生成NaCl、2ClO2、Cl2、H2O,化学方程式为:2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O,每生成1molClO2需要消耗NaClO3 1mol,同时生成氯气0.5mol,结合电子守恒氯化钠电解槽内反应为Cl-+3H2O$\frac{\underline{\;通电\;}}{\;}$ClO3-+3H2↑,每生成1molNaClO3 ,同时生成3mol氢气.
解答 解:根据流程图可知道:食盐水在特定条件下电解得到氯酸钠(NaClO3)、氢气,NaClO3和HCl反应,生成ClO2、氯气和氯化钠,b气体为氯气,a气体为氢气,
A.分析可知a为氢气,b为氯气,故A错误;
B.电解食盐水得到氯酸钠(NaClO3)和H2,电解的离子反应方程式为:Cl-+3H2O$\frac{\underline{\;通电\;}}{\;}$ClO3-+3H2↑,氯化钠电解槽内每生成2 mol a气体,转移4mol e-,故B错误;
C.ClO2发生器中的反应为,化学方程式NaClO3和盐酸发生歧化反应,生成NaCl、ClO2、Cl2、H2O,阴极是ClO3-得到电子生成ClO2,电极反应为ClO3-+2H++e-═ClO2↑+H2O,故C错误;
D.NaClO3和盐酸发生歧化反应,生成NaCl、2ClO2、Cl2、H2O,化学方程式为:2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O,每生成1molClO2需要消耗NaClO3 1mol,同时生成氯气0.5mol,结合电子守恒氯化钠电解槽内反应为Cl-+3H2O$\frac{\underline{\;通电\;}}{\;}$ClO3-+3H2↑,每生成1molNaClO3 ,同时生成3mol氢气,为使ab气体恰好完全反应,理论上每生成1molClO2需要补充2.5mol氯气,故D正确;
故选D.
点评 本题考查了电解原理的分析、电解产物判断、电子守恒的计算应用,主要是流程分析和反应原理的理解,掌握基础是解题关键,题目难度较大.

 名校课堂系列答案
名校课堂系列答案| A. | 银氨溶液 | B. | 乙酸溶液 | C. | 氯化铁溶液 | D. | 氢氧化钠溶液 |
| A. | 通入了1 molCl2的新制氯水中,HClO、Cl-、C1O-粒子数之和为2NA | |
| B. | 标准状况下,22.4L NH3和HCl的混合气体中含有的分子总数为NA | |
| C. | 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02NA | |
| D. | 高温下,0.3mol Fe与足量的水蒸气完全反应失去的电子数为0.8NA |
 磷酸铁锂(LiFePO4)电池是一种高效、环保的新型电池,装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐,电池工作时的总反应为:LiFePO4+6C $?_{放电}^{充电}$Li1-xFePO4+LixC6,则下列说法错误的是( )
磷酸铁锂(LiFePO4)电池是一种高效、环保的新型电池,装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐,电池工作时的总反应为:LiFePO4+6C $?_{放电}^{充电}$Li1-xFePO4+LixC6,则下列说法错误的是( )| A. | 装置中的聚合物隔膜应为阳离子交换膜 | |
| B. | 充电时,Li+迁移方向为由右向左 | |
| C. | 充电时,LiFePO4中的铁元素被氧化 | |
| D. | 放电时,正极的电极反应式为:Li1-xFePO4+xLi++xe-═LiFePO4 |
| A. | 2 molSO2与3 molO2反应生成的SO3分子数为2NA | |
| B. | 30 g乙酸和葡萄糖混合物中的氢原子数为2NA | |
| C. | 常温下pH=12的NaOH溶液中,水电离出的氢离子数为10-12NA | |
| D. | 标准状况下,2.24 L C2H6含有的共价键数为0.6NA |
| A. | 适当升高温度能促进FeCl3水解 | |
| B. | 加水稀释能促进其水解,并提高Fe(OH)3的浓度 | |
| C. | 加少量浓盐酸能促进FeCl3水解 | |
| D. | 保存氯化铁溶液时应加入少量铁粉 |
Ⅰ.制取氧化锌主要工艺如图1:
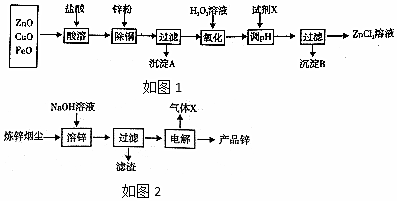
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
| A. | 石油裂解和蛋白质水解都是由高分子化合物生成小分子物质的过程 | |
| B. | 乙烯分别使溴水和酸性KMnO4溶液褪色,反应原理相同 | |
| C. | C6H14有5种同分异构体 | |
| D. | CH4和Cl2按体积比1:3混合可制得纯净的CHCl3 |