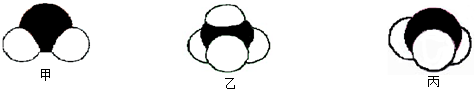
��Ŀ����
������Ԫ��A��B��C��Dԭ������������������ֻ��һ��Ϊ����Ԫ�أ�A��Cͬ���壬B������������Ϊ������3����B��C������������֮����D��������������ȣ���1��д��D������������Ӧˮ����Ļ�ѧʽ ��
��2��C2B2�ĵ���ʽΪ �����к��еĻ�ѧ������Ϊ ��
��3������������Ԫ���е��������ֿ���������ֳ��������ˮ��Һ���Լ��ԣ�D�ĵ��ʿ���������һ�ֻ����ﷴӦ��������һ�ֻ����д���÷�Ӧ�����ӷ���ʽ ��
��4����ʯī�缫���CD�ı�����Һ����Ӧ�����ӷ���ʽΪ ��
��5����ͨ��״���£���1gA������D������ȼ������AD����ʱ�ų�92.3kJ��������2mol AD������ȫ�ֽ�����A�����D������Ȼ�ѧ����ʽΪ ��
���𰸡�������B������������Ϊ������3����ӦΪOԪ�أ�B��C������������֮����D��������������ȣ�B������������Ϊ6����C������������ӦΪ1��D������������Ϊ7����CӦΪNa��DӦΪCl��A��Cͬ���壬��AӦΪH����϶�Ӧ���ʡ�������Ľṹ�����ʽ����⣮
����⣺B������������Ϊ������3����ӦΪOԪ�أ�B��C������������֮����D��������������ȣ�B������������Ϊ6����C������������ӦΪ1��D������������Ϊ7����CӦΪNa��DӦΪCl��A��Cͬ���壬��AӦΪH������AΪH��BΪO��CΪNa��DΪCl����
��1��DΪCl������������Ӧˮ����ΪHClO4���ʴ�Ϊ��HClO4��
��2��BΪO��CΪNa����Ӧ�Ļ�����ΪNa2O2��Ϊ���ӻ�����������Ӽ��ͷǼ��Թ��ۼ�������ʽΪ ��
��
�ʴ�Ϊ�� �����Ӽ��ͷǼ��Թ��ۼ���
�����Ӽ��ͷǼ��Թ��ۼ���
��3������Ԫ���γɵ�ˮ��Һ���Լ��ԵĻ�������NaOH��NaClO������Cl2��NaOH��Ӧ����NaClO����Ӧ�����ӷ���ʽΪCl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��4����ⱥ��NaCl��Һ�����ӷ���ʽΪ2Cl-+2H2O Cl2+H2+2OH-��
Cl2+H2+2OH-��
�ʴ�Ϊ��2Cl-+2H2O Cl2+H2+2OH-��
Cl2+H2+2OH-��
��5��n��H2��=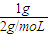 =0.5mol���ų�92.3kJ��������1molH2��Ӧ����2molHCl�ų�184.6kJ������
=0.5mol���ų�92.3kJ��������1molH2��Ӧ����2molHCl�ų�184.6kJ������
2molHCl�ֽ�ʱ����Ҫ����184.6kJ������
��Ӧ���Ȼ�ѧ����ʽΪ2HCl��g���TH2��g��+Cl2��g����H=+184.6kJ/mol��
�ʴ�Ϊ��2HCl��g���TH2��g��+Cl2��g����H=+184.6kJ/mol��
���������⿼��ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�Ѷ��еȣ�����ע�����ԭ�Ӻ�������Ų��ص㣬����ԭ�ӽṹ�����ƶ�Ԫ�ص����࣬������������ʵĽṹ�������Լ��绯ѧ���Ȼ�ѧ����ʽ�Ŀ��飬ѧϰ�л���ͬѧ�ǰ������֪ʶ��������Ӧ�ã�
����⣺B������������Ϊ������3����ӦΪOԪ�أ�B��C������������֮����D��������������ȣ�B������������Ϊ6����C������������ӦΪ1��D������������Ϊ7����CӦΪNa��DӦΪCl��A��Cͬ���壬��AӦΪH������AΪH��BΪO��CΪNa��DΪCl����
��1��DΪCl������������Ӧˮ����ΪHClO4���ʴ�Ϊ��HClO4��
��2��BΪO��CΪNa����Ӧ�Ļ�����ΪNa2O2��Ϊ���ӻ�����������Ӽ��ͷǼ��Թ��ۼ�������ʽΪ
 ��
���ʴ�Ϊ��
 �����Ӽ��ͷǼ��Թ��ۼ���
�����Ӽ��ͷǼ��Թ��ۼ�����3������Ԫ���γɵ�ˮ��Һ���Լ��ԵĻ�������NaOH��NaClO������Cl2��NaOH��Ӧ����NaClO����Ӧ�����ӷ���ʽΪCl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��4����ⱥ��NaCl��Һ�����ӷ���ʽΪ2Cl-+2H2O
 Cl2+H2+2OH-��
Cl2+H2+2OH-���ʴ�Ϊ��2Cl-+2H2O
 Cl2+H2+2OH-��
Cl2+H2+2OH-����5��n��H2��=
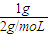 =0.5mol���ų�92.3kJ��������1molH2��Ӧ����2molHCl�ų�184.6kJ������
=0.5mol���ų�92.3kJ��������1molH2��Ӧ����2molHCl�ų�184.6kJ������2molHCl�ֽ�ʱ����Ҫ����184.6kJ������
��Ӧ���Ȼ�ѧ����ʽΪ2HCl��g���TH2��g��+Cl2��g����H=+184.6kJ/mol��
�ʴ�Ϊ��2HCl��g���TH2��g��+Cl2��g����H=+184.6kJ/mol��
���������⿼��ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�Ѷ��еȣ�����ע�����ԭ�Ӻ�������Ų��ص㣬����ԭ�ӽṹ�����ƶ�Ԫ�ص����࣬������������ʵĽṹ�������Լ��绯ѧ���Ȼ�ѧ����ʽ�Ŀ��飬ѧϰ�л���ͬѧ�ǰ������֪ʶ��������Ӧ�ã�

��ϰ��ϵ�д�
�����Ŀ