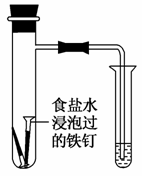
题目内容
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3===FeCO3↓+Na2SO4
FeCO3+C6H8O7===FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
(1)制备FeCO3时,选用的加料方式是________(填字母,)原因是________________________________________________________________________。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是________________________________________________________________________________________________________________________________________________。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。
①铁粉的作用是______________________________________________ _____________________。
②反应结束后,无需过滤,除去过量铁粉的方法是________________________________________________________________________________________________________________________________________________。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是________________________________________________________________________。
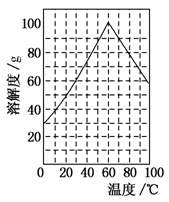
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合上图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应,__________________________________________________________________________________________________________________________________,得到FeSO4溶液,_________________________________ _____________________________________________,得到FeSO4·7H2O晶体。
解析 (1)碳酸钠溶液水解显碱性,Fe2+在碱性环境中会生成氢氧化亚铁沉淀,故应在硫酸亚铁中加入碳酸钠溶液。(2)检验FeCO3沉淀是否洗涤干净,即检验洗涤液中是否含有SO ,可以用酸化的氯化钡溶液检验,若无白色沉淀产生,则表明已洗涤干净。(3)Fe2+具有还原性,易被空气中的氧气氧化,加入铁粉可以防止其被氧化。铁可与酸(柠檬酸)反应,故可用柠檬酸直接处理多余的铁粉,使之生成柠檬酸亚铁。(4)加入乙醇可以抑制柠檬酸亚铁在水中的溶解,提高柠檬酸亚铁的产率。(5)硫铁矿烧渣与稀硫酸反应,生成硫酸铁和硫酸铝,二氧化硅不溶于稀硫酸,故接下来的操作是“过滤”,滤液中含有铁离子和铝离子,向滤液中加入足量的强碱,铁离子以沉淀的形式析出,铝元素以偏铝酸根离子的形式存在于溶液中,再过滤,滤渣为氢氧化铁,加硫酸得到硫酸铁,然后再加铁粉生成硫酸亚铁;最后加热浓缩、冷却结晶、过滤、洗涤、低温干燥,即得硫酸亚铁晶体(绿矾)。
,可以用酸化的氯化钡溶液检验,若无白色沉淀产生,则表明已洗涤干净。(3)Fe2+具有还原性,易被空气中的氧气氧化,加入铁粉可以防止其被氧化。铁可与酸(柠檬酸)反应,故可用柠檬酸直接处理多余的铁粉,使之生成柠檬酸亚铁。(4)加入乙醇可以抑制柠檬酸亚铁在水中的溶解,提高柠檬酸亚铁的产率。(5)硫铁矿烧渣与稀硫酸反应,生成硫酸铁和硫酸铝,二氧化硅不溶于稀硫酸,故接下来的操作是“过滤”,滤液中含有铁离子和铝离子,向滤液中加入足量的强碱,铁离子以沉淀的形式析出,铝元素以偏铝酸根离子的形式存在于溶液中,再过滤,滤渣为氢氧化铁,加硫酸得到硫酸铁,然后再加铁粉生成硫酸亚铁;最后加热浓缩、冷却结晶、过滤、洗涤、低温干燥,即得硫酸亚铁晶体(绿矾)。
答案 (1)c 避免生成Fe(OH)2沉淀
(2)取最后一次的洗涤滤液1~2 mL于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净
(3)①防止+2价的铁元素被氧化 ②加入适量柠檬酸让铁粉反应完全
(4)降低柠檬酸亚铁在水中的溶解量,有利于晶体析出
(5)“过滤,向反应液中加入足量的铁粉,充分搅拌后,滴加NaOH溶液调节反应液的pH约为5,过滤”或“过滤,向滤液中滴加过量的NaOH溶液,过滤,充分洗涤固体,向固体中加入足量稀硫酸至固体完全溶解,再加入足量的铁粉,充分搅拌后,过滤” (滴加稀硫酸酸化),加热浓缩得到60 ℃饱和溶液,冷却至0 ℃结晶,过滤,少量冰水洗涤,低温干燥

 优等生题库系列答案
优等生题库系列答案煤气化是有效利用化石能源手段之一,有关反应如下:
 |
获得的气体称为水煤气。某研究性学习小组为探究气体的成分进行了如下实验:
【实验】使水蒸气通过灼热的焦炭,收集反应后流出的气体。
【提出假设】对气体的成份提出了三种假设。
假设1:该气体是CO、H2 假设2:该气体是C0、H2、H20。(
⑴假设3: ______________________________________
【设计实验方案,验证假设】
他们拟用T图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设(加热装置和导管等在图中略去,实验前P置内部的空气已经排尽)。

(2 )按气流从左至右连接各仪器,用题中小写字母表示接口连接顺序(仪器可重复使用)混合气
→dc →_______→_______→ij →_______→_______→_______→ij;
(3) 仪器A中需加入试剂的是____________,其中反应的化学方程式是
______________________________________________________________;
(4) 仪器B中需加入试剂的名称是_______________,其作用是_________________________;
(5)本实验的尾气需要处理,处理的方法为:____________________________________,
(6) 某同学认为增加焦炭的量可以提高化学反应①的速率,你是否同意他的说法,并简述理由___________________________________________________________________________