题目内容
请按下列要求规范答题
(1)
H、
H、
H 互为 ,16O2、18O3 互为 .
A.同位素 B.相同物质
C.同素异形体 D.同分异构体
(2)某元素的最高价氧化物分子式R2O5,已知R的气态氢化物中含氢8.82%,则R的相对原子量约为 ,R元素周期表中的位置为 .
(3)铷和另一种碱金属形成的合金7.8g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是: .(铷的相对原子量取85.5)
(4)质量相同的H2O和D2O与足量钠反应,放出的气体在标况下的体积之比为 .
(1)
1 1 |
2 1 |
3 1 |
A.同位素 B.相同物质
C.同素异形体 D.同分异构体
(2)某元素的最高价氧化物分子式R2O5,已知R的气态氢化物中含氢8.82%,则R的相对原子量约为
(3)铷和另一种碱金属形成的合金7.8g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是:
(4)质量相同的H2O和D2O与足量钠反应,放出的气体在标况下的体积之比为
考点:同位素及其应用,位置结构性质的相互关系应用
专题:原子组成与结构专题,元素周期律与元素周期表专题
分析:(1)根据质子数相同,而中子数不同的原子互为同位素;由同种元素形成的不同种单质互为同素异形体;
(2)化合物中正负化合价的代数和为0,由“某元素的最高价氧化物分子式R2O5”可知,元素R的化合价为+5价;则它跟氢生成的氢化物的化学式为RH3,根据氢化物中含氢为8.82%,可以计算出R的相对原子质量;元素的原子序数=质子数=核外电子数,根据原子的核外电子排布以及主族元素周期数=电子层数、主族族序数=最外层电子数;
(3)钾和另一种碱金属在化合物中的化合价均为+1价,由2M+2H2O═2MOH+H2↑,计算金属的摩尔质量,利用平均摩尔质量的来解答;
(4)质量相同的H2O和D2O分别与足量的金属钠反应,由2H2O(D2O)~H2↑来计算氢气的体积关系.
(2)化合物中正负化合价的代数和为0,由“某元素的最高价氧化物分子式R2O5”可知,元素R的化合价为+5价;则它跟氢生成的氢化物的化学式为RH3,根据氢化物中含氢为8.82%,可以计算出R的相对原子质量;元素的原子序数=质子数=核外电子数,根据原子的核外电子排布以及主族元素周期数=电子层数、主族族序数=最外层电子数;
(3)钾和另一种碱金属在化合物中的化合价均为+1价,由2M+2H2O═2MOH+H2↑,计算金属的摩尔质量,利用平均摩尔质量的来解答;
(4)质量相同的H2O和D2O分别与足量的金属钠反应,由2H2O(D2O)~H2↑来计算氢气的体积关系.
解答:
解:(1)
H、
H、
H是质子数相同,中子数不同的原子,互为同位素;16O2、18O3 是由氧元素形成的不同单质;
故选:A;C;
(2)由“某元素的最高价氧化物分子式R2O5”可知,元素R的化合价为+5价;则它的氢化物的化学式为RH3,设R的相对原子质量为x,则
×100%=8.82%,解得:x=31,该元素为磷元素,原子序数为15,原子结构示意图为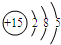 ,由3个电子层,处于第三周期,最外层电子数为5,处于ⅤA族,故该元素处于第三周期第ⅤA族;
,由3个电子层,处于第三周期,最外层电子数为5,处于ⅤA族,故该元素处于第三周期第ⅤA族;
故答案为:31;第三周期第ⅤA族;
(3)氢气的物质的量为
=0.1mol,
由2M+2H2O═2MOH+H2↑,
2 1
0.2mol 0.1mol
则金属的平均摩尔质量为
=39g/mol,
铷的摩尔质量为85.5g/mol,则另一种碱金属的摩尔质量一定小于39g/mol,所以另一碱金属可能是Li或
Na;
故答案为:Li或Na;
(4)质量相同的H2O和D2O的物质的量之比为
:
=10:9,由关系式:2H2O(D2O)~H2↑可知气体体积之比等于水的物质的量之比;
故答案为:10:9.
1 1 |
2 1 |
3 1 |
故选:A;C;
(2)由“某元素的最高价氧化物分子式R2O5”可知,元素R的化合价为+5价;则它的氢化物的化学式为RH3,设R的相对原子质量为x,则
| 3 |
| x+3 |
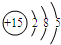 ,由3个电子层,处于第三周期,最外层电子数为5,处于ⅤA族,故该元素处于第三周期第ⅤA族;
,由3个电子层,处于第三周期,最外层电子数为5,处于ⅤA族,故该元素处于第三周期第ⅤA族;故答案为:31;第三周期第ⅤA族;
(3)氢气的物质的量为
| 0.2g |
| 2g/mol |
由2M+2H2O═2MOH+H2↑,
2 1
0.2mol 0.1mol
则金属的平均摩尔质量为
| 7.8g |
| 0.2mol |
铷的摩尔质量为85.5g/mol,则另一种碱金属的摩尔质量一定小于39g/mol,所以另一碱金属可能是Li或
Na;
故答案为:Li或Na;
(4)质量相同的H2O和D2O的物质的量之比为
| 1 |
| 18 |
| 1 |
| 20 |
故答案为:10:9.
点评:本题是道综合题,涉及知识点较多,注意平均摩尔质量法的运用,难度不大.

练习册系列答案
相关题目
M是一种常见的大气污染物,其在空气中的含量是环境空气质量的重要测评指标.该气体具有漂白性,能使品红溶液褪色,加热后溶液颜色又能恢复.M的化学式为( )
| A、SO2 |
| B、CO2 |
| C、HCl |
| D、NO |
根据原子序数,下列各组原子能以离子键相结合的是( )
| A、6与8 | B、6与14 |
| C、8与16 | D、8与11 |

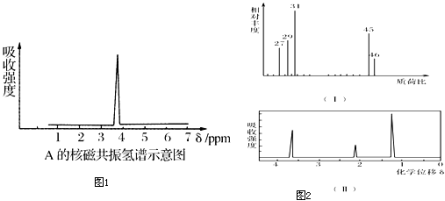
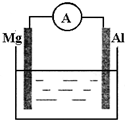 如图所示装置:
如图所示装置: