题目内容
19.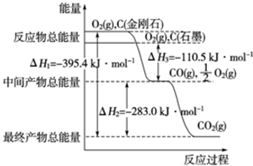 金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示.
金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示.(1)在通常状况下,金刚石和石墨石墨(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式C(石墨,s)═C(金刚石,s)△H=+1.9kJ•mol-1.
(2)12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量252.0kJ.
(3)已知在常温常压下:
①CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-359.8kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-556.0kJ•mol-1
③H2O(g)=H2O(l)△H=-44.0kJ•mol-1
写出体现甲醇燃烧热的热化学方程式CH3OH(l)+3O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ•mol-1.
分析 (1)依据物质能量越高,越活泼分析判断,依据图象能量变化写出石墨转化为金刚石的热化学方程式,反应是吸热反应;
(2)依据极值计算判断生成的气体组成,结合热化学方程式计算得到;
(3)根据盖斯定律,由已知热化学方程式构造目标热化学方程式.
解答 解:(1)图象分析金刚石能量高于石墨,能量越低越稳定,所以说明石墨稳定,图象分析石墨转化为金刚石需要吸收热量=395.4KJ-393.5KJ=1.9KJ;反应的热化学方程式为C(石墨,s)═C(金刚石,s)△H=+1.9 kJ•mol-1
故答案为:石墨;C(石墨,s)═C(金刚石,s)△H=+1.9 kJ•mol-1;
(2)12g石墨物质的量为1mol,在一定量空气中燃烧,依据元素守恒,若生成二氧化碳质量为44g,若生成一氧化碳质量为28g,生成气体36g,28g<36g<44g,判断生成的气体为一氧化碳和二氧化碳气体,设一氧化碳物质的量为x,二氧化碳物质的量为(1-x)mol,28x+44(1-x)=36g,x=0.5mol,二氧化碳物质的量为0.5mol;依据图象分析,C(石墨,s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 ;C(石墨,s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5 kJ•mol-1
生成二氧化碳和一氧化碳混合气体放出热量=393.5 kJ•mol-1 ×0.5mol+110.5 kJ•mol-1 ×0.5mol=252KJ;12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为252.0kJ;
故答案为:252.0 kJ;
(3)已知:①CH3OH(l)+O2(g)═CO(g)+2H2O(g);△H=-359.8kJ•mol-1
②2CO(g)+O2(g)═2CO2(g);△H=-556.0kJ•mol-1
③H2O(g)═H2O(l);△H=-44.0kJ•mol-1
根据盖斯定律:①+$\frac{1}{2}$×②+2×③得CH3OH(l)+3O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ•mol-1;
故答案为:CH3OH(l)+3O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ•mol-1.
点评 本题考查了化学反应与能量、盖斯定律、物质稳定性的判断、键能的计算,侧重于学生的分析、计算能力的考查,为高频考点,题目难度中等,注意把握盖斯定律的含义及其应用方法.

 名校课堂系列答案
名校课堂系列答案| A. | 灼热的炭与二氧化碳反应 | B. | 铁和稀硫酸的反应 | ||
| C. | 硝酸铵溶于水 | D. | 钢铁制品的生锈 |
| A. | 金、铜、铁 | B. | 铁、铜、金 | C. | 铁、金、铜 | D. | 铜、金、铁 |
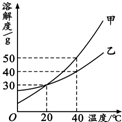
| A. | 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数 | |
| B. | 40℃时,分别在100 g水中加入40 g甲、乙,所得溶液溶质的质量分数相等 | |
| C. | 40℃时,分别在100 g水中加入30 g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液 | |
| D. | 20℃时,分别在100 g水中加入40 g甲、乙,加热到40℃时,乙溶液为饱和溶液 |
| A. | 氧化铁可制作防锈油漆 | |
| B. | 碳酸氢钠可制作焙制糕点的发酵粉 | |
| C. | 氯气不能用来合成药物,因为它有毒 | |
| D. | NO能促进血管扩张,防止血管栓塞 |
| A. | 0 | B. | $\frac{1}{4}$ | C. | $\frac{1}{2}$ | D. | $\frac{3}{4}$ |
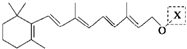
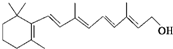 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.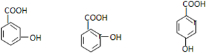 .
.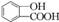 .
.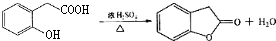 .
.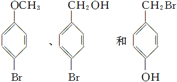 .
.