��Ŀ����
����Ŀ����ͬԪ�ص�ԭ���ڷ������������ӵ�������С����һ��ֵX����ʾ����XԽ����ԭ���������ӵ�����Խǿ�������γɵķ����г�Ϊ�����һ����������ijЩ������Ԫ�ص�Xֵ��
Ԫ�� | Li | Be | B | C | O | F |
Xֵ | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
Ԫ�� | Na | Al | Si | P | S | Cl |
Xֵ | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
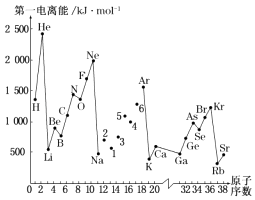
��1��ͨ������Xֵ�ı仯���ɣ�ȷ��N��Mg��Xֵ��Χ����X��Mg������ ��X��N���� ��
��2���Ʋ�Xֵ��ԭ�Ӱ뾶�Ĺ�ϵ�� ��
��3��ij�л���ṹ��ʽΪ ![]() ����S��N�У�����Ϊ���õ��Ӷ�ƫ��˭����дԭ�����ƣ���
����S��N�У�����Ϊ���õ��Ӷ�ƫ��˭����дԭ�����ƣ���
��4��������ɸ������ǵ��ɼ�����ԭ����ӦԪ�ص縺�ԵIJ�ֵ��X��1.7ʱ��һ��Ϊ���Ӽ�������X��1.7ʱ��һ��Ϊ���ۼ������ƶ�AlBr3�л�ѧ����������
��5��Ԥ��Ԫ�����ڱ��У�Xֵ��С��Ԫ��λ����������Ԫ�س��⣩��
���𰸡�
��1��0.93��1.57��2.55��3.44
��2��ͬ���ڣ���ͬ���壩Ԫ�أ�xֵԽ��ԭ�Ӱ뾶ԽС
��3����
��4�����ۼ�
��5���������ڵڢ�A��
���������⣺��1���ɱ�����ֵ�ɿ�����ͬ������Ԫ�ص�xֵ��ԭ�Ӱ뾶�ļ�С������ͬ�������϶���xֵ��С��xֵ�ı仯���������Եı仯���ʣ�0.93��x��Mg����1.57��2.55��x��N����3.44�� ���Դ��ǣ�0.93��1.57��2.55��3.44����2���ɱ�����ֵ�ɿ�����ͬ������Ԫ�ص�xֵ��ԭ�Ӱ뾶�ļ�С������ͬ�������϶���ԭ�Ӱ뾶����xֵ��С�����Դ��ǣ�ͬ���ڣ���ͬ���壩Ԫ�أ�xֵԽ��ԭ�Ӱ뾶ԽС����3���Ա����ڱ��жԽ���λ�õ�Xֵ��֪��X��B����X��Si����X��C����X��P����X��O����X��Cl���������֪��X��N����X��S��������S��N�У����õ��Ӷ�Ӧƫ��ԭ�ӣ����Դ��ǣ�������4�����֪��AlCl3�ġ�X=1.55��1.7����X��Br����X��Cl��������AlBr3�ġ�XӦС��AlCl3�ģ�Ϊ���ۼ������Դ��ǣ����ۼ�����5�����ݵݱ���ɣ�Xֵ��С��ӦΪCs��FrΪ������Ԫ�أ�λ�ڵ������ڡ��ڢ�A�壬���Դ��ǣ��������ڵڢ�A�壮

 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д�����Ŀ�������ֶ�����Ԫ�أ����ǵĽṹ�����ʵ���Ϣ���±�������
Ԫ�� | �ṹ�����ʵ���Ϣ |
A | �Ƕ������У���ϡ�������⣩ԭ�Ӱ뾶����Ԫ�أ���Ԫ�ص�ij�ֺϽ���ԭ�ӷ�Ӧ�ѵĵ��ȼ� |
B | B��Aͬ���ڣ�������������ˮ��������� |
C | Ԫ�ص���̬�⻯�K������ˮ������������� |
D | �Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ���� |
����ݱ�����Ϣ��д��
��1��Aԭ�ӵĺ�������Ų�ʽ ��
��2��BԪ�������ڱ��е�λ�������Ӱ뾶��BA������ڡ���С�ڡ�����
��3��Cԭ�ӵĵ����Ų�ͼ�� �� ��ԭ�Ӻ�������δ�ɶԵ��ӣ�������ߵĵ���Ϊ����ϵĵ��ӣ��������Σ�
��4��Dԭ�ӵĵ����Ų�ʽΪ �� D���Ľṹʾ��ͼ�� ��
��5��B������������Ӧ��ˮ������A������������Ӧ��ˮ���ﷴӦ�Ļ�ѧ����ʽΪ��D���⻯���ˮ���ﷴӦ�Ļ�ѧ����ʽΪ ��