题目内容
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为29.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C、D的第一电离能由小到大的顺序为 .
(2)C的氢化物分子式是
(3)D-的离子结构示意图是 .
(4)E元素原子的核外电子排布式是 .
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)C的氢化物分子式是
(3)D-的离子结构示意图是
(4)E元素原子的核外电子排布式是
考点:位置结构性质的相互关系应用
专题:
分析:D原子得到一个电子后3p轨道全充满,原子的电子排布式应为1S22S22P63S23P5,为Cl元素,A+比D原子形成的离子少一个电子层,则A应为Na元素;C与A形成A2C型离子化合物,则C应为第ⅥA主族元素,根据核电荷数A<B<C<D<E可知C应为S元素,E的原子序数为29,为Cu元素;B原子的p轨道半充满,结合核电荷数大小关系可知其电子排布式应为:1S22S22P63S23P3,则B为P元素,据此进行解答.
解答:
解:D原子得到一个电子后3p轨道全充满,原子的电子排布式应为1S22S22P63S23P5,为Cl元素,A+比D原子形成的离子少一个电子层,则A应为Na元素;C与A形成A2C型离子化合物,则C应为第ⅥA主族元素,根据核电荷数A<B<C<D<E可知C应为S元素,E的原子序数为29,为Cu元素;B原子的p轨道半充满,结合核电荷数大小关系可知其电子排布式应为:1S22S22P63S23P3,则B为P元素,
(1)在元素周期表中,同一周期元素的第一电离能从左到右逐渐增大,同一主族元素的第一电离能从上到下逐渐减小,据此可判断四种元素的第一电离能的顺序为:Na<S<P<Cl,
故答案为:Na<S<P<Cl;
(2)C的氢化物为硫化氢,其分子式为:H2S,故答案为:H2S;
(3)D为Cl元素,氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构,则氯离子的离子结构示意图为: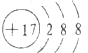 ,
,
故答案为: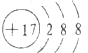 ;
;
(4)E为Cu,原子核外电子数为29,根据能量最低原理,核外电子排布式为:1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1.
(1)在元素周期表中,同一周期元素的第一电离能从左到右逐渐增大,同一主族元素的第一电离能从上到下逐渐减小,据此可判断四种元素的第一电离能的顺序为:Na<S<P<Cl,
故答案为:Na<S<P<Cl;
(2)C的氢化物为硫化氢,其分子式为:H2S,故答案为:H2S;
(3)D为Cl元素,氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构,则氯离子的离子结构示意图为:
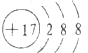 ,
,故答案为:
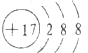 ;
;(4)E为Cu,原子核外电子数为29,根据能量最低原理,核外电子排布式为:1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1.
点评:本题考查位置、结构与性质关系的应用,题目难度中等,涉及元素推断题、核外电子排布、电负性等知识,推断出元素的种类是解答本题的关键,注意掌握原子结构与元素周期律、元素周期表的关系.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
A、MnO2 与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、铜与稀硝酸反应:Cu+4H++2NO3-═2H2O+Cu2++2NO2↑ | ||||
| C、足量氨水吸收少量二氧化硫气体:NH3?H2O+SO2=NH4++HSO3- | ||||
| D、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
验证某有机物属于烃,应完成的实验内容的是( )
| A、只测定它的C、H原子个数比 |
| B、只要证明它完全燃烧后产物只有H2O和CO2 |
| C、只测定其燃烧产物中H2O和CO2的物质的量之比 |
| D、只测定该试样的质量及试样完全燃烧后生成H2O和CO2的质量 |
将下列各种物质分别与适量的溴水混合并振荡,静置后,混合液分两层,溴水层几乎呈无色的是( )
| A、食盐水 | B、乙烯 | C、苯 | D、戊烯 |
下列物质均有漂白性,其中漂白原理与其他三种不同的是( )
| A、HClO |
| B、SO2 |
| C、O3 |
| D、Na2O2 |
某同学用下列装置制备并检验Cl2的性质.下列说法错误的是( )
A、 即使MnO2过量,盐酸也不能全部消耗 |
B、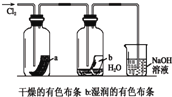 湿润的有色布条能褪色 |
C、 生成棕色的烟 |
D、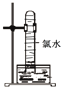 用光照射氯水后液体颜色加深 |
下列事实能证明甲烷分子是以碳原子为中心的正四面体结构的是( )
| A、四个C-H键完全相同 |
| B、CH4的一氯代物只有一种 |
| C、在常温常压下CH2Cl2为液体 |
| D、CH2Cl2只有一种空间结构 |
以下自发反应能用△H判据来解释的是( )
| A、硝酸铵自发地溶于水 |
| B、2N2O5(g)=4NO2 (g)+O2(g)△H=+156.7kJ/mol |
| C、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)△H=+74.9 kJ/mol |
| D、2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
