题目内容
4.下列4种物质熔点沸点由高到低排列为①>④>③>②(填序号)①金刚石(C-C)②锗(Ge-Ge)③晶体硅(Si-Si)④金刚砂(Si-C)
分析 原子晶体中熔沸点高低与键长成反比,键长越长晶体熔沸点越低,键长Ge-Ge>Si-Si>Si-C>C-C,据此分析解答.
解答 解:原子晶体中熔沸点高低与键长成反比,键长越长晶体熔沸点越低,这几种物质都是原子晶体,键长Ge-Ge>Si-Si>Si-C>C-C,所以物质的熔沸点高低顺序是 ①>④>③>②,故答案为:①>④>③>②.
点评 本题考查晶体熔沸点高低判断,明确原子晶体熔沸点高低与键长关系即可解答,知道常见晶体类型的判断方法及熔沸点高低判断方法,题目难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
19.某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿氏常数,下列说法中正确的是( )
| A. | 氧元素的相对原子质量为$\frac{12a}{b}$ | B. | 1mol该原子质量为aNAg | ||
| C. | x g该氧原子所含的电子数为$\frac{8x}{a}$ | D. | y g 该氧原子的中子数一定为$\frac{8y}{a}$ |
13.下列离子方程式中,不正确的是( )
| A. | C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| B. | C6H5OH+OH-→C6H5O-+H2O | |
| C. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O |
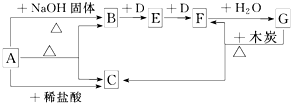
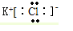 ;CO2
;CO2

 .
.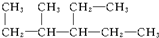 6
6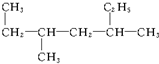 7
7 6
6 6.
6.