籾朕坪否
20⤴書嗤〙CH3COOH、〖HCl、〗H2SO4 眉嶽卑匣⇧喘會催指基和双諒籾⦿↙1⇄輝万断pH屢揖扮⇧凪麗嵎議楚敵業議喇寄欺弌電双頁〙﹅〖﹅〗
↙2⇄輝万断議麗嵎議楚敵業屢揖扮⇧凪pH議喇寄欺弌電双頁〙﹅〖﹅〗
↙3⇄嶄才揖匯付珠卑匣⇧俶揖敵業議眉嶽磨卑匣議悶持購狼葎〙=〖﹅〗
↙4⇄悶持才pH屢揖議〙、〖、〗眉卑匣⇧蛍艶嚥怎楚仗頚郡哘⇧屢揖訳周和恢伏狽賑議悶持購狼葎〙﹅〖=〗⤴
蛍裂 ↙1⇄pH屢揖卑匣嶄狽宣徨敵業屢揖⇧閑磨頁匯圷樋磨⇧葬磨頁屈圷膿磨、冦磨頁匯圷膿磨⇧象緩登僅◉
↙2⇄敵業屢揖⇧卑匣pH嚥卑匣嶄狽宣徨敵業撹郡曳◉
↙3⇄嶄才吉楚狽剳晒墜⇧嶧払揖敵業磨議悶持嚥磨窮宣竃恷嶮狽宣徨議敵業撹郡曳◉
↙4⇄pH屢揖卑匣嶄狽宣徨敵業屢揖⇧閑磨頁匯圷樋磨⇧葬磨頁屈圷膿磨、冦磨頁匯圷膿磨⇧功象恷嶮嬬窮宣議狽宣徨議悳楚蛍裂⤴
盾基 盾⦿↙1⇄pH屢揖卑匣嶄狽宣徨敵業屢揖⇧閑磨頁匯圷樋磨⇧葬磨頁屈圷膿磨、冦磨頁匯圷膿磨⇧邪譜狽宣徨敵業葎1mol/L⇧夸閑磨敵業寄噐1mol/L、冦磨敵業頁1mol/L、葬磨敵業頁0.5mol/L⇧侭參凪麗嵎議楚敵業議喇寄欺弌電双頁 〙﹅〖﹅〗◉
絞基宛葎⦿〙﹅〖﹅〗◉
↙2⇄輝万断議麗嵎議楚敵業屢揖扮⇧邪譜脅頁1mol/L⇧閑磨嶄狽宣徨敵業弌噐1mol/L、葬磨嶄狽宣徨敵業頁2mol/L、冦磨嶄狽宣徨敵業頁1mol/L⇧狽宣徨敵業埆寄pH埆弌⇧侭參凪pH議喇寄欺弌電双頁〙﹅〖﹅〗◉
絞基宛葎⦿〙﹅〖﹅〗◉
↙3⇄嶄才吉楚狽剳晒墜⇧嶧払揖敵業磨議悶持嚥磨窮宣竃恷嶮狽宣徨議敵業撹郡曳⇧眉嶽卑匣敵業屢吉⇧葬磨頁屈圷磨、閑磨才冦磨脅頁匯圷磨⇧侭參恷嶮窮宣竃狽宣徨議敵業葬磨﹅閑磨=冦磨⇧侭參嶧債眉嶽磨議悶持寄弌乏會頁〙=〖﹅〗⇧
絞基宛葎⦿〙=〖﹅〗◉
↙4⇄pH屢揖卑匣嶄狽宣徨敵業屢揖⇧閑磨頁匯圷樋磨⇧葬磨頁屈圷膿磨、冦磨頁匯圷膿磨⇧邪譜狽宣徨敵業葎1mol/L⇧夸閑磨敵業寄噐1mol/L、冦磨敵業頁1mol/L、葬磨敵業頁0.5mol/L⇧蛍艶嚥怎楚仗頚郡哘⇧冦磨嚥葬磨郡哘伏撹議狽賑屢揖⇧屢揖訳周和恢伏狽賑議悶持購狼葎〙﹅〖=〗⇧
絞基宛葎⦿〙﹅〖=〗⤴
泣得 云籾深臥磨珠詞栽卑匣協來登僅⇧迦嶷深臥僥伏蛍裂、容僅嬬薦⇧苧鳩匯圷磨、屈圷磨才珠議協楚購狼頁盾云籾購囚⇧籾朕佃業嶄吉⇧迦嶷噐深臥僥伏議蛍裂嬬薦才哘喘嬬薦⤴

 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛| A⤴ | NaCl NaBr NaI | B⤴ | NaCl NaBr | C⤴ | NaCl NaI | D⤴ | NaCl |
| A⤴ | 械梁械儿和⇧4.4g厰肌侭根σ囚方朕葎0.7NA | |
| B⤴ | 炎彈彜趨和⇧5.6LCO2嚥怎楚Na2O2郡哘廬卞議窮徨方葎0.5 NA | |
| C⤴ | 12g墳朝路↙汽蚊墳朝⇄嶄根嗤鎗圷桟議倖方葎0.5NA | |
| D⤴ | 50ml敵業葎18.4mol•L-1敵葬磨嚥怎楚有裏犯郡哘⇧伏撹SO2蛍徨議方朕葎0.46NA |
| A⤴ | 磨來卑匣嶄音贋壓匯邦栽葦蛍徨 | |
| B⤴ | 蓮瞥pH=3議閑磨⇧卑匣嶄侭嗤宣徨敵業譲週詰 | |
| C⤴ | 械梁和⇧pH譲葎10議NaOH卑匣才NaCN卑匣嶄⇧喇邦窮宣竃栖議H+敵業屢吉 | |
| D⤴ | 﨑狽剳晒綻議傅彷匣嶄紗富楚議邦⇧峠財﨑卑盾圭﨑卞強拝c↙Mg2+⇄音延 |
| A⤴ | 什悶嶄蛍柊嵎腺徨議岷抄寄噐卑匣嶄蛍柊嵎議腺徨岷抄 | |
| B⤴ | 﨑吋才議柁晒鑓卑匣嶄紗秘狽剳晒墜卑匣誼欺碕砦弼柿牛 | |
| C⤴ | 苧君‐KAl↙SO4⇄2•12H2O/辛參恂昌邦質 | |
| D⤴ | 狽剳晒鑓卑什、蓮狭習、堝零吉譲醤嗤供器櫛孖嵆 |
| A⤴ | 嶄來卑匣嶄⦿K+、Fe3+、SO42-、Cl- | |
| B⤴ | 邦窮宣議c↙H+⇄=1〜10-13mol/L議卑匣嶄⦿K+、Na+、[Al↙OH⇄4]-、CO32- | |
| C⤴ | 嚥Al郡哘嬬慧竃H2議卑匣嶄⦿Fe2+、Na+、NO3-、SO42- | |
| D⤴ | $\frac{{K}_{W}}{c↙{H}^{+}⇄}$=1〜10-13mol/L議卑匣嶄⦿K+、Cu2+、Cl-、NO3- |
〙
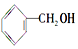
〖
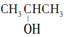
〗CH3OH
∠
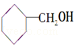
⊥
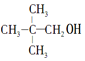
⌒

| A⤴ | 〙∠⊥ | B⤴ | 〖∠ | C⤴ | 〖⌒ | D⤴ | 〙〖⌒ |
