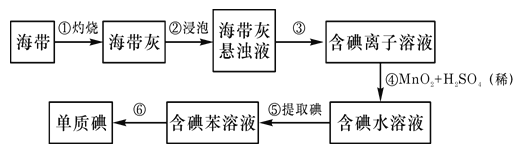
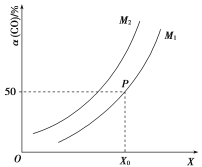
题目内容
【题目】某兴趣小组用下图装置探究氨的催化氧化。
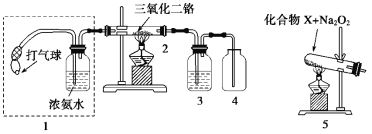
(1)氨催化氧化的化学方程式为____。
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是__(填“吸热”或“放热”)反应。
(3)为实现氨催化氧化,也可用装置5替换装置1,若化合物X为NH4HCO3,NH4HCO3发生分解反应,该反应的化学方程式为___,部分产物和Na2O2反应得到O2,使NH3和O2混合催化氧化,装置4中可以观察到有红棕色气体生成,红棕色气体生成的化学方程式为___。
(4)为保证在装置4中观察到红棕色气体,装置3中应装入___。若取消装置3,在装置4中会观察到产生大量白烟,该白烟的化学式是___。
【答案】4NH3+5O2![]() 4NO+6H2O 放热 NH4HCO3
4NO+6H2O 放热 NH4HCO3![]() NH3↑+CO2↑+H2O 2NO+O2=2NO2 浓H2SO4 NH4NO3
NH3↑+CO2↑+H2O 2NO+O2=2NO2 浓H2SO4 NH4NO3
【解析】
(1)氨催化氧化,生成一氧化氮和水。
(2)停止加热后仍能保持红热,该反应能继续释放维持反应进行的热量。
(3)若化合物X为NH4HCO3,NH4HCO3发生分解反应,则生成氨气、二氧化碳和水,二氧化碳和水能与Na2O2反应得到O2,使NH3和O2混合催化氧化,装置4中可以观察到有红棕色气体生成,红棕色气体由一氧化氮与氧气反应生成。
(4)为保证在装置4中观察到红棕色气体,装置3中应装入去除氨气的物质。若取消装置3,在装置4中会观察到产生大量白烟,该白烟应为氨气与硝酸反应的产物。
(1)氨催化氧化,生成一氧化氮和水,方程式为4NH3+5O2![]() 4NO+6H2O。答案为:4NH3+5O2
4NO+6H2O。答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(2)停止加热后仍能保持红热,说明该反应放热。答案为:放热;
(3)若化合物X为NH4HCO3,NH4HCO3发生分解反应,NH4HCO3![]() NH3↑+CO2↑+H2O,后续反应为:2Na2O2+2H2O==4NaOH+O2↑,2Na2O2+2CO2==2Na2CO3+O2,4NH3+5O2
NH3↑+CO2↑+H2O,后续反应为:2Na2O2+2H2O==4NaOH+O2↑,2Na2O2+2CO2==2Na2CO3+O2,4NH3+5O2![]() 4NO+6H2O,2NO+O2==2NO2。答案为:NH4HCO3
4NO+6H2O,2NO+O2==2NO2。答案为:NH4HCO3![]() NH3↑+CO2↑+H2O;2NO+O2=2NO2;
NH3↑+CO2↑+H2O;2NO+O2=2NO2;
(4)为保证在装置4中观察到红棕色气体,装置3中应装入去除氨气的物质,以应使用浓H2SO4。若取消装置3,在装置4中会观察到产生大量白烟,则发生反应为3NO2+H2O==2HNO3+NO,NH3+HNO3=NH4NO3(白烟)。答案为:浓H2SO4;NH4NO3。

【题目】一定温度下,体积为2 L的密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如下表:
物质 | X | Y | Z |
初始物质的量/mol | 0.2 | 0.2 | 0 |
平衡物质的量/mol | 0.1 | 0.05 | 0.1 |
下列说法正确的是( )
A.反应可表示为![]() ,其平衡常数为8 000
,其平衡常数为8 000
B.增大压强使平衡向生成Z的方向移动,则平衡常数增大
C.若将容器的体积压缩至1 L,则X的体积分数减小,浓度增大
D.若升高温度,Z的浓度增大,则温度升高时![]() 正增大,
正增大,![]() 逆减小
逆减小
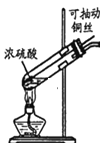
【题目】某小组同学用如图装置进行铜与浓硫酸反应时,发现试管中有黑色物质产生。同学猜测,黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学继续进行实验探究,获得数据如表。下列说法不正确的是
硫酸浓度/ mol·L﹣1 | 黑色物质出现的温度∕℃ | 黑色物质消失的温度∕℃ |
15 | 约150 | 约236 |
16 | 约140 | 约250 |
18 | 约120 | 不消失 |
A.硫酸浓度越大,黑色物质越易出现、越难消失
B.黑色物质消失过程中有SO2、H2S生成
C.硫酸浓度为16 mol·L﹣1时,先升温至250℃以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质
D.取黑色物质洗涤、干燥后,加稀硫酸充分混合,固体质量不变,说明黑色物质中不含CuO