题目内容
8分)CH4分子在空间呈四面体形状,1个C原子与4个H原子各共用一对电子对形成4条共价键,如图所示为一个正方体,已画出1个C原子(在正方体中心)、1个H原子(在正方体顶点)和1条共价键(实线表示),请画出另3个H原子的合适位置和3条共价键,任意两条共价键夹角的余弦值为__________。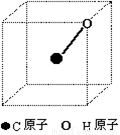
【答案】
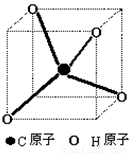 π-arccos1/3
π-arccos1/3
【解析】
试题分析:由于碳原子在正方体中心,一个氢原子在顶点,因为碳氢键是等长的,那么另三个氢原子也应在正方体的顶点上,正方体余下的七个顶点可分成三类,三个为棱的对侧,三个为面对角线的对侧,一个为体对角线的对侧。显然三个在面对角线对侧上的顶点为另三个氢原子的位置,所以键角伟π-arccos1/3。
考点:考查甲烷分子结构的有关判断和计算
点评:该题是中等难度的试题,试题基础性强,侧重考查学生的能力,试题难易适中。主要是有利于培养学生的空间想象能力以及严谨的逻辑推理能力。

练习册系列答案
相关题目