题目内容
11.物质A、B、C的转化关系如图所示:
①若A 为常见金属,C为淡黄色固体,C与水反应生成D,则D的电子式为
 .
.②若A分子含有10个电子且有刺激性气味的气体,则A的结构式为
 ,写出A生成B的反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,写出A生成B的反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.③若A为黄绿色气体,X为常见金属单质,C溶液为浅绿色,则X元素在周期表中的位置第四周期Ⅷ族;写出B与X反应的化学方程式2FeCl3+Fe=3FeCl2.
分析 ①若A 为常见金属,C为淡黄色固体,则过氧化钠,所以A为钠,B为氧化钠,X为氧气,C与水反应生成D为氢氧化钠;
②若A分子含有10个电子且有刺激性气味的气体,A能连续与X反应,则A为氨气,氨气与氧气反应生成B为一氧化氮,一氧化氮与氧气反应生成C为二氧化氮,所以X为氧气;
③若A为黄绿色气体,则A为氯气,X为常见金属单质,C溶液为浅绿色,X为铁,C为氯化亚铁,氯化亚铁与氯气反应生成B为氯化铁,据此答题.
解答 解:①若A 为常见金属,C为淡黄色固体,则过氧化钠,所以A为钠,B为氧化钠,X为氧气,C与水反应生成D为氢氧化钠,氢氧化钠的电子式为 ,
,
故答案为: ;
;
②若A分子含有10个电子且有刺激性气味的气体,A能连续与X反应,则A为氨气,氨气与氧气反应生成B为一氧化氮,一氧化氮与氧气反应生成C为二氧化氮,所以X为氧气,氨气的结构式为 ,A生成B的反应方程式为4NH3+5O2 $\frac{\underline{催化剂}}{△}$ 4NO+6H2O,
,A生成B的反应方程式为4NH3+5O2 $\frac{\underline{催化剂}}{△}$ 4NO+6H2O,
故答案为: ;4NH3+5O2 $\frac{\underline{催化剂}}{△}$ 4NO+6H2O;
;4NH3+5O2 $\frac{\underline{催化剂}}{△}$ 4NO+6H2O;
③若A为黄绿色气体,则A为氯气,X为常见金属单质,C溶液为浅绿色,X为铁,C为氯化亚铁,氯化亚铁与氯气反应生成B为氯化铁,铁元素在周期表中第四周期Ⅷ族,B与X反应的化学方程式为 2FeCl3+Fe=3FeCl2,
故答案为:第四周期Ⅷ族; 2FeCl3+Fe=3FeCl2.
点评 本题考查无机物推断,难度中等,熟练掌握元素化合物的性质是关键,侧重考查学生对常见物质性质的掌握,掌握一种物质能与另一种物质连续两步反应在化学中所涉及的元素是本题的难点.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
1.下列做法正确的是( )
| A. | 用手接触药品 | |
| B. | 用嘴吹灭酒精灯 | |
| C. | 洒在桌面上的酒精燃烧,立即用湿抹布盖灭 | |
| D. | 将带有溶液的滴管平放在实验台上 |
2.下列溶液氯离子的物质的量浓度与50mL 1mol•L-1AlCl3溶液中氯离子的物质的量浓度相等的是( )
| A. | 150 mL3 mol•L-1氯酸钠溶液 | B. | 75 mL 3 mol•L-1氯化钙溶液 | ||
| C. | 150 mL 3 mol•L-1氯化钾溶液 | D. | 50 mL 3 mol•L-1氯化镁溶液 |
19.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-=Mg2+ | |
| B. | 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ | |
| C. | 正极反应式为Ag++e-=Ag | |
| D. | 电池放电时Cl-由正极向负极迁移 |
6.己知维生素A的结构简式可写为 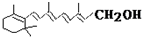 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H32O | |
| B. | 维生素A不能使溴的四氯化碳溶液褪色 | |
| C. | 该有机物能发生取代反应 | |
| D. | 1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应 |
16.下列生活生产中常见的物质里含有的有机物属于高分子化合物的是( )
| A. | 蜂蜜中含有的葡萄糖 | B. | 石油中含有的C16H34 | ||
| C. | 芹菜中含有的纤维素 | D. | 植物油中含有的油脂 |
3.化学与生活密切相关.下列说法不正确的是( )
| A. | 乙烯可用作水果的催熟剂 | |
| B. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 | |
| C. | 二氧化硫可用作食品的漂白剂 | |
| D. | 交警可用酸性重铬酸钾来检测司机是否酒驾 |
15.如表,已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,常温下其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | +1 | -4 | -2 | -1 |
| A. | 乙的常见氧化物有两种 | |
| B. | 气态氢化物稳定性:丙<丁 | |
| C. | 丙的氧化物能与戊的氢化物的水溶液反应 | |
| D. | 原子半径大小:甲>丙 |