题目内容
2.A、B、C、D、E是五种气态烃,其中A、B、C能使溴水褪色.1摩尔A与2摩尔氯气完全加成.A与C、B与E分别同系物,A在催化剂存在下与氢气反应可得到B,在同温同压下B与氮气的密度相同,D是最简单的有机物,C、E没有同类的异构体,则五种气态烃的名称分别是:乙炔、乙烯、1,3-丁二烯、甲烷、环丙烷.分析 A、B、C、D、E是五种气态烃,其中A、B、C能使溴水褪色,在同温同压下Y与氮气的密度相同,则B为乙烯,D是最简单的有机物,则D为甲烷,B与E为同系物,E没有同类的异构体,则E为环丙烷,A在催化剂存在下与氢气反应可得到B,则A为乙炔,1molC与2mol氯气完全加成,生成物分子中每个碳原子上都连有氢原子和氯原子,A与C为同系物,则C为1,3-丁二烯,据此答题.
解答 解:A、B、C、D、E是五种气态烃,其中A、B、C能使溴水褪色,在同温同压下Y与氮气的密度相同,则B为乙烯,结构简式为CH2=CH2,D是最简单的有机物,则D为甲烷,结构简式为CH4,B与E分别具有相同的分子通式,E没有同类的异构体,则E为环丙烷,结构简式为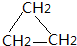 ,A在催化剂存在下与氢气反应可得到B,则A为乙炔,结构简式为CH≡CH,1molC与2mol氯气完全加成,生成物分子中每个碳原子上都连有氢原子和氯原子,A与C具有相同的分子通式,则C为1,3-丁二烯,结构简式为CH2=CH-CH2=CH2,综上所述:A为乙炔,B为乙烯,C为1,3-丁二烯,D为甲烷,E为环丙烷,
,A在催化剂存在下与氢气反应可得到B,则A为乙炔,结构简式为CH≡CH,1molC与2mol氯气完全加成,生成物分子中每个碳原子上都连有氢原子和氯原子,A与C具有相同的分子通式,则C为1,3-丁二烯,结构简式为CH2=CH-CH2=CH2,综上所述:A为乙炔,B为乙烯,C为1,3-丁二烯,D为甲烷,E为环丙烷,
故答案为:乙炔、乙烯、1,3-丁二烯、甲烷、环丙烷.
点评 本题主要考查烃的组成与性质,难度不大,注意根据物质的性质和组成特点进行物质推断,本题有利于基础知识的巩固.

练习册系列答案
相关题目
11.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是Ar(填元素符号)
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式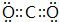 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ | VⅡA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)②③⑦三种元素的原子半径从大到小的顺序为Cl>N>O(填元素符号)
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式HClO4,碱性最强的化合物的名称氢氧化钾.
(4)元素⑤的氧化物与元素④的最高价氧化物对应水化物反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O.
(5)元素⑥和⑦形成的气态氢化物较稳定是HCl(填化学式),用方程式来说明元素⑦的非金属性比⑥的非金属强的事实Cl2+H2S=S↓+2HCl(一个或两个方程式均可)
(6)表示①与③形成的化合物的电子式
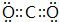 ,写出它的一种用途做灭火剂等.
,写出它的一种用途做灭火剂等.
13.室温下由水电离出的H+的浓度是1×10-12mol/L,则该溶液( )
| A. | 一定是酸性溶液 | B. | 一定是碱性溶液 | ||
| C. | 可能是中性溶液 | D. | 可能是酸性溶液也可能是碱性溶液 |
10.下列各项叙述中,正确的是( )
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 24Cr原子的电子排布式是1s22s22p63s23p63d44s2 | |
| C. | 所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
17.下列物质中不属于混合物的是( )
| A. | C4H10 | B. | 溴乙烷 | C. | 聚乙烯 | D. | 天然气 |
7.下列叙述正确的是( )
| A. | 实验室可通过蒸馏的方法除去自来水中含有的氯离子等杂质制蒸馏水 | |
| B. | 将氢氧化钠稀溶液逐滴滴入氯化铁饱和溶液中,边滴边搅拌,可获得氢氧化铁胶体 | |
| C. | 由于氢氧化铁胶体带正电,所以电泳时阴极颜色加深 | |
| D. | 浓硫酸不慎溅到皮肤上,应该立即用大量水冲洗,然后涂上稀NaOH溶液 |
14.下列说法错误的是( )
| A. | 从1L 1 mol•L-1 的氯化钠溶液中取出10ml后,其浓度仍是1 mol•L-1 | |
| B. | NaHSO4溶液与NaOH溶液反应的离子方程式:H++OH-═H2O | |
| C. | 黄河入海口处三角洲的形成与胶体性质无关 | |
| D. | 氧化剂具有氧化性,在化学反应中化合价降低,发生还原反应 |
11.25℃和1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g)△H=+56.76kJ/mol,该反应能自发进行的原因是( )
| A. | 是吸热反应 | B. | 是放热反应 | C. | 是熵减少的反应 | D. | 是熵增大的反应 |