��Ŀ����
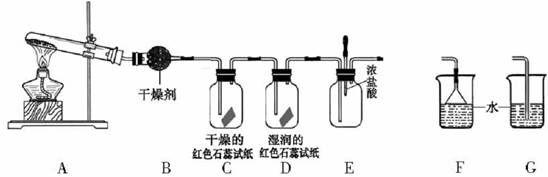
ij��ѧ��ѧ�о���ѧϰС����������װ����ȡ��̽�����������ʡ�

(1)A�еĻ�ѧ��Ӧ����ʽ�� ��
(2)Aװ�û���������ȡ���� ��ֻ��һ�֣�
(3)����21.4gNH4Cl���壬������ȡNH3����״����������� L (NH4C1��Ħ������Ϊ53.5g��mol-1����
(4)ʵ�����ռ������ķ�����
(5)C��Dװ������ɫ�ᷢ���仯���� ���C����D����
(6)��ʵ�����һ��ʱ���ѹEװ���еĽ�ͷ�ιܣ�����1-2��Ũ���ᣬ�ɹ۲쵽��������
(7)Ϊ��ֹ����������ɿ�����Ⱦ����Ҫ������װ�õ�ĩ������һ��β������װ�ã����ʵ�װ���� ���F����G������
(8����ʯ����ˮ���÷ų�������ʵ�������ô�ԭ��������ʯ���еμ�Ũ��ˮ�����Կ�����ȡ����������Ϊ��ʯ�ҿ������� ���ʴ��棨����ţ���
A����ʯ�ң�NaOH��CaO�Ĺ������
B.NaOH ����
C��������Һ
D��ʯ��ʯ����CaCO3)
����11�֣�
��1��2NH4Cl + Ca(OH)2 CaCl2 + 2NH3��+ 2H2O ��2�֣�
CaCl2 + 2NH3��+ 2H2O ��2�֣�
��2��O2��������������������Ҳ���֣���1�֣� ��3��8.96 ��2�֣�
��4�������ſ����� ��1�֣� ��5��D ��1�֣�
��6���а������� ��1�֣� ��7��F ��1�֣� ��8��A B ��2�֣�
��������
���������(1) A������ȡ����������ʽΪ2NH4Cl + Ca(OH)2 CaCl2 + 2NH3��+ 2H2O��
CaCl2 + 2NH3��+ 2H2O��
(2)��+������ʵ��װ�ã���������ȡ������
(3)���������غ㣬21.4gNH4Cl��0.4mol���ʰ���Ҳ��0.4mol�����Ϊ8.96L��
(4)������������ˮ���ܶ�С�ڿ��������ռ������ķ����������ſ�������
(5)��������ˮ���ܳʼ��ԣ�����ɫ�仯����D��
(6)������Ũ���Ἣ������Ӧ�������Ȼ�粒��壬�����а������ɵ�����
(7)Fװ���ܷ�ֹ������G�����ԣ���ѡFװ�á�
(8��C���������ԣ��Ͱ�����Ӧ���ʴ���D������ȣ��ʴ�����ѡAB��
���㣺ʵ������ȡ�����˼· ��������ķ���װ�ú��ռ�װ����ѡȡ����
��������1���������ڿ���ͬѧ�ǶԳ��û�ѧ�������˽��ʶ�������ֻ�кܺõ���ʶ���ǣ���ʵ����ܵ���Ӧ�֡���2��������չ�����⣬���ڿ���������ʵķ�Ӧ��ͷ�Ӧ����ѡȡװ�á���3����������Ϣ����ͻ�ƿڣ��ҳ���Ӧ��������д��ѧ����ʽ��





 CaCl2 + 2NH3��+ 2H2O
CaCl2 + 2NH3��+ 2H2O