题目内容
4.等物质的量的氢气和二氧化碳气体在同温同压下具有相同的( )| A. | 原子数 | B. | 体积 | C. | 密度 | D. | 质量 |
分析 A.氢气分子、二氧化碳分子含有原子数目分别为2、3;
B.同温同压下,气体体积之比等于其物质的量之比;
C.同温同压下,气体密度之比等于其相对分子质量之比;
D.根据m=nM判断.
解答 解:A.氢气分子、二氧化碳分子含有原子数目分别为2、3,等物质的量的氢气和二氧化碳气体含有原子数目不相等,含有原子数目之比为2:3,故A错误;
B.同温同压下,气体体积之比等于其物质的量之比,等物质的量的氢气和二氧化碳气体在同温同压下具有相同的体积,故B正确;
C.同温同压下,气体密度之比等于其相对分子质量之比,则氢气和二氧化碳气体在同温同压下密度之比为2:44=1:22,密度不相等,故C错误;
D.氢气与二氧化碳摩尔质量不相等,根据m=nM可知,等物质的量的氢气和二氧化碳气体的质量不相等,故D错误,
故选:B.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列表示正确的是( )
| A. | CH4的球棍模型示意图为 | B. | H2O2的电子式: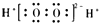 | ||
| C. | 葡萄糖的最简式为CH2O | D. | 聚丙烯的结构简式: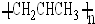 |
15.下列说法不正确的是( )
| A. | 天津港爆炸案中对剧毒的氰化钠(NaCN) 喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| B. | 碳酸钙分解、氢氧化钡晶体和氯化铵固体反应、高温下铝与氧化铁反应都是吸热反应 | |
| C. | 刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 | |
| D. | 石油原油的脱水,有色玻璃、纳米材料、塑料、橡胶及合成纤维等制造过程都会用到胶体 |
12.下列离子方程式书写正确的是( )
| A. | 向50mL 1mol•L-1明矾溶液中滴入少量0.1mol•L-1Ba(OH)2溶液Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| B. | 已知还原性Fe2+>Br-,a mol FeBr2溶液中通入a mol Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4Cl- | |
| C. | 向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I-═3I2+2H2O | |
| D. | 在澄清石灰水中加入适量碳酸氢镁溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
9.下列电离方程式中,正确的是( )
| A. | NaHCO3=Na++HCO3- | B. | H2SO4?2H++SO42- | ||
| C. | NaHSO3=Na++H++SO32- | D. | 熔融状态下:NaHSO4=Na++H++SO42- |
16.从硫粉和铁粉的混合物中提取硫,最合理的方法是( )
| A. | 用磁铁分离出混合物中的铁粉 | B. | 将混合物溶于二硫化碳后过滤 | ||
| C. | 将混合物溶解于稀盐酸后过滤 | D. | 将混合物加热升华 |
6.下列关于金属元素特征的叙述中,正确的是( )
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
| A. | .①②③ | B. | ②③ | C. | ① | D. | 全部 |
7.下列元素在自然界中仅以化合态存在的是( )
①Si ②Al ③Cl ④Fe ⑤Na.
①Si ②Al ③Cl ④Fe ⑤Na.
| A. | ①②⑤ | B. | ①② | C. | ①②③ | D. | ①②③④⑤ |