题目内容
9.下列电离方程式中,正确的是( )| A. | NaHCO3=Na++HCO3- | B. | H2SO4?2H++SO42- | ||
| C. | NaHSO3=Na++H++SO32- | D. | 熔融状态下:NaHSO4=Na++H++SO42- |
分析 A.碳酸氢钠是强碱弱酸盐,属于强电解质在水溶液中电离出钠离子和碳酸氢根离子;
B.硫酸是强酸属于强电解质,水溶液中完全电离生成氢离子和硫酸根离子;
C.亚硫酸氢钠是强碱弱酸盐,属于强电解质完全电离生成钠离子和亚硫酸氢根离子;
D.硫酸氢钠是强酸强碱盐由钠离子和硫酸氢根离子构成,熔融状态完全电离生成钠离子和硫酸氢根离子;
解答 解:A.碳酸氢钠是强碱弱酸盐,水溶液中电离出钠离子和碳酸氢根离子,电离方程式为NaHCO3=Na++HCO3-,故A正确;
B.硫酸水溶液中完全电离生成氢离子和硫酸根离子,电离方程式为:H2SO4=2H++SO42-,故B错误;
C.亚硫酸氢钠完全电离生成钠离子和亚硫酸氢根离子,电离方程式为NaHSO3=Na++HSO3-,故C错误;
D.硫酸氢钠熔融状态完全电离生成钠离子和硫酸氢根离子,电离方程式为:NaHSO4=Na++HSO4-,故D错误;
故选A.
点评 本题考查了物质结构和性质,主要是电离出离子的分析判断,注意硫酸氢钠熔融状态电离出的阴离子为硫酸氢根离子,题目较简单.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
19.下列有关物质浓度关系的描述中,正确的是( )
| A. | 25℃时,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7mol•L-1 | |
| B. | 25℃时,向0.1mol•L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) | |
| C. | 0.1mol•L-1的NaHCO3溶液中:c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) | |
| D. | 同温下,pH相同时,溶液物质的量浓度:c(CH3COONa)>c(NaHCO3)>c(Na2CO3)>c(C6H5ONa) |
20.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,28 g N2所含电子数为10NA | |
| B. | 46 g钠充分燃烧时转移电子数为2NA | |
| C. | 0.1 mol•L-1NH4Cl溶液中Cl-离子数为0.1NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA |
17.下列叙述正确的是( )
| A. | 分子式为C3H6有机物最多存在3个C-C单键,与C4H10的碳碳单键数相同 | |
| B. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双健 | |
| C. | 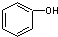 和 C7H8O分子组成相差一个-CH2-,因此是同系物关系 和 C7H8O分子组成相差一个-CH2-,因此是同系物关系 | |
| D. | 分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以确定有机物结构简式为C2H5-OH |
4.等物质的量的氢气和二氧化碳气体在同温同压下具有相同的( )
| A. | 原子数 | B. | 体积 | C. | 密度 | D. | 质量 |
14. 甲醇是重要的化工原料,在化工生产中有广泛的应用.
甲醇是重要的化工原料,在化工生产中有广泛的应用.
(1)已知反应:CO(g)+2H2(g)?CH3OH(g)△H=Q
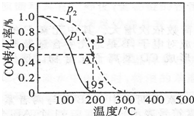
在20L的密闭容器中,按物质的量之比1:2充入CO和H2,测得CO的转化率随温度及压强的变化如下图所示,P2及195℃时n(H2)随时间的变化如表所示:
①O~3min,平均速率V(CH3OH)=O.033mo1•L-1•min-1,Q<0(填“<”“=”或“>”).
②图中压强(P1、P2)的大小顺序为P1<P2,理由是相同温度下,增大压强CO转化率提高.
③在P2及195℃时,该反应的平衡常数K=25.
 甲醇是重要的化工原料,在化工生产中有广泛的应用.
甲醇是重要的化工原料,在化工生产中有广泛的应用.(1)已知反应:CO(g)+2H2(g)?CH3OH(g)△H=Q
在20L的密闭容器中,按物质的量之比1:2充入CO和H2,测得CO的转化率随温度及压强的变化如下图所示,P2及195℃时n(H2)随时间的变化如表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
②图中压强(P1、P2)的大小顺序为P1<P2,理由是相同温度下,增大压强CO转化率提高.
③在P2及195℃时,该反应的平衡常数K=25.
1.用0.10mol/L H2SO4溶液滴定0.1mol/L的氨水,滴定的过程中不可能出现的结果是( )
| A. | c(NH4+)>c(SO42-),c(OH-)>c(H+) | B. | c(NH4+)=c(SO42-),c(OH-)=c(H+) | ||
| C. | c(NH4+)>c(SO42-),c(H+)>c(OH-) | D. | c(SO42-)>c(NH4+),c(H+)>c(OH-) |
11.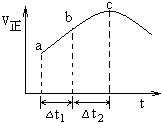 向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
 向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )| A. | 该反应为放热反应 | |
| B. | 反应物浓度:c>b>a | |
| C. | a、b均未建立平衡,c点恰好达到平衡 | |
| D. | 若在恒温恒容容器中,以相同的投料进行该反应,平衡后转化率小于绝热恒容容器中的转化率 |
12.下列仪器通常不能用于物质分离的是( )
| A. | 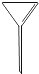 | B. |  | C. | 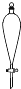 | D. |  |