题目内容
锌锰废电池经处理后,生产并回收硫酸锌及碳酸锰,其中生产工业级碳酸锰工艺如下:
试回答下列问题:
(1)锰在元素周期表中位于第________周期,第________族。
(2)步骤1和步骤2是将MnO2转化为MnO并溶于硫酸,其中步骤2中的氢气,是另一个流程产生的副产品,请写出产生氢气的反应方程式__________________________。
(3)步骤3和步骤4都是除杂质。
①X是一种“绿色”氧化剂,则X是________(填化学式)。
②步骤3是除去杂质Fe2+。请用文字和必要的方程式简述除去Fe2+的方法(已知三种离子沉淀的pH范围为Fe3+:2.7~3.7,Mn2+:8.6~10.1,Fe2+:7.6~9.6)_________________________________________________________。
③步骤4中主要反应方程式为:MeSO4+BaS=MeS↓+BaSO4↓(Me主要为Pb、Cd、Hg等),则其除去杂质的原理是_________________________________________________。
(4)已知进行步骤5的操作时,溶液3(主要成分为MnSO4)会产生大量无色无味的气泡,则步骤5反应的化学方程式为_______________________________________。
(1)四 ⅦB
(2)Zn+H2SO4=ZnSO4+H2↑
(3)①H2O2 ②在酸性条件下加入双氧水,将Fe2+氧化成Fe3+、2Fe2++H2O2+2H+=2Fe3++2H2O,调节pH至3.7~8.6,使Fe3+沉淀完全,Fe3++3H2O??Fe(OH)3+3H+ ③以BaS为沉淀剂,使Pb2+、Cd2+、Hg+等金属离子,生成更难溶的硫化物而除去
(4)MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+H2O+CO2↑
解析

 阅读快车系列答案
阅读快车系列答案对下列过程中发生反应的叙述正确的是
| A.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| B.Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质 |
| C.从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应 |
| D.从海水中提取溴单质的过程所涉及的反应均为置换反应 |
海水中镁的总储量约为2.1×1015t,目前世界上60%的镁来自海水,工业规模海水提镁的流程如图所示:
试回答下列问题:
(1)海水提镁的过程中①、②反应的化学方程式:
①_____________________________________,
②______________________________________。
(2)由氯化镁溶液制取无水氯化镁固体,其操作过程是____________________
(3)为了使MgSO4完全转化为Mg(OH)2,则加入的生石灰要过量,然后分离得Mg(OH)2沉淀,考虑Ca(OH)2溶解度,应该用________法分离。
(4)金属镁、铝的工业冶炼方法既有相似之处,又有不同之别,下表是氧化镁和氯化镁的熔沸点数据:
| 物质 | 氧化镁 | 氯化镁 |
| 熔点(℃) | 2 852 | 714 |
| 沸点(℃) | 3 600 | 1 412 |
工业上炼镁采用电解熔融氯化镁,而冶炼铝则用电解熔融的Al2O3,其原因是____________________________________
Ⅰ下列说法不正确的是____ 。
| A.可以利用某些炼钢废渣来生产磷肥 |
| B.具有永久硬度的水主要用加热的方法来进行软化 |
| C.硫酸工业中,在接触室安装热交换器是为了利用S03转化为H2S04时放出的热量 |
| D.合成氨工业原料气净化时,常用碳酸钾溶液吸收除去二氧化碳 |
请回答下列问题:
(1)用离子交换膜电解饱和食盐水时,精制的饱和食盐水应该加入到 极室。
(2)已知在离子交换膜电解槽中,理论上每小时通过1安培的直流电,每槽可以产生1.492 g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342×103 kg/m3)113 m3,电解槽的电流强度1.45×l04 A,该电解槽的电解效率为 。
(3)示意图中制取NaHC03的化学方程式为 。
(4)有人提出直接加热Mg(OH)2得到Mg0,再电解熔融Mg0得金属Mg,这样可简化流程。请判断该方案是否可行,并说明理由 。
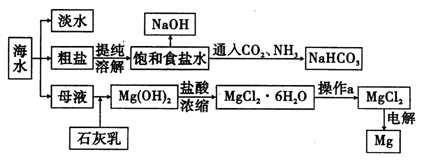
下图是某工厂对海水资源进行综合利用的示意图。
请回答下列问题:
(1)请列举一种海水淡化的方法 。
(2)工业上常用离子交换膜电解槽生产NaOH,电解过程中大量通过离子交换膜的离子是 ,NaOH在电解槽的 室生成,由饱和食盐水制取NaOH的化学方程式为 。
(3)侯氏制碱法中向饱和食盐水中通入CO2和NH3制得NaHCO3,先通入 (填化学式),理由是 。再由NaHCO3制得纯碱,化学方程式为 。
(4)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取。已知有关物质的熔沸点数据如下:
| | MgO | MgCl2 |
| 熔点/℃ | 2 852 | 714 |
| 沸点/℃ | 3 600 | 1 412 |
结合表中数据和实际生产情况说明,工业上生产镁采用电解MgCl2而不是电解MgO的理由 。


 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓