题目内容
下列离子方程式表示正确的是A.在澄清石灰水中加入过量碳酸氢钠溶液:
Ca2++OH-+HCO![]() ==CaCO3↓+H2O
==CaCO3↓+H2O
B.过量CO2气体通入NaClO溶液中:
H2O+CO2+2ClO-==CO![]() +2HClO
+2HClO
C.硫酸铵和氢氧化钡溶液共热:
NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D.二氧化锰和浓盐酸共热:
MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D
解析:A项石灰水中加入过量碳酸氢钠溶液时,Ca2+与OH-物质的量之比应符合1∶2,Ca2++2OH-+2HCO![]() ==CaCO3↓+CO
==CaCO3↓+CO![]() +2H2O,A错。B项过量CO2通入NaClO溶液中生成NaHCO3和HClO,离子方程式为H2O+CO2+ClO-==HCO
+2H2O,A错。B项过量CO2通入NaClO溶液中生成NaHCO3和HClO,离子方程式为H2O+CO2+ClO-==HCO![]() +HClO,故B不正确。C项漏掉Ba2++SO
+HClO,故B不正确。C项漏掉Ba2++SO![]() ==BaSO4↓,故C错。D项浓HCl常用的浓度为37.5%,所以盐酸应写成离子形式,D正确。
==BaSO4↓,故C错。D项浓HCl常用的浓度为37.5%,所以盐酸应写成离子形式,D正确。

练习册系列答案
相关题目
 NH3H2O+H+
NH3H2O+H+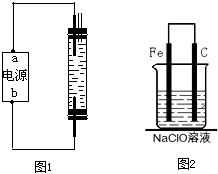 (2010?烟台一模)2008年5月12日我国四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒液,如NaClO溶液.某校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究.
(2010?烟台一模)2008年5月12日我国四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒液,如NaClO溶液.某校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究.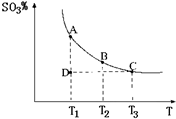 (2011?松江区模拟)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
(2011?松江区模拟)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义. 2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题: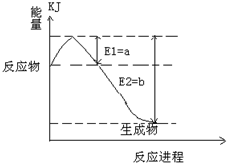

 研究化学反应原理对于生产、生活及环境保护具有重要意义.
研究化学反应原理对于生产、生活及环境保护具有重要意义.