��Ŀ����
 �о���ѧ��Ӧԭ�����������������������������Ҫ���壮
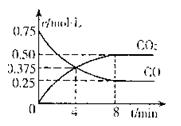
�о���ѧ��Ӧԭ�����������������������������Ҫ���壮��I����ҵ������Ĺ����д��ڷ�Ӧ��2SO2��g��+O2?2SO3��g����T0��ʱ����2mol SO2��1.5mol O2����2L�ܱ������з���������Ӧ��������SO2�����ʵ������� �ȱ仯��������ͼ��ʾ��
��ͼ��a�������Ӧ����
��������������֤��������Ӧ�Ѿ��ﵽ��ѧƽ��״̬����
a����λʱ��������1molO2��ͬʱ����2molS03
b��������S02��O2��SO3��Ũ��֮��Ϊ2��1��2
C��������ѹǿ���ֲ���
d����������ƽ����Է����������ֲ���
��T1��ʱ��������Ӧ�Ļ�ѧƽ�ⳣ��K=
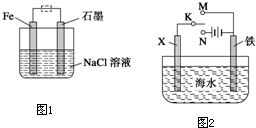
��2��̼�����һ�ֳ��õ��̬���ʣ���ˮ��Һ�Լ��ԣ���ԭ����
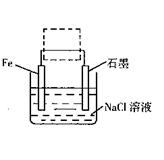
��3������ˮ���ؽ���������Ⱦʱ������Ͷ����������ؽ�������ת��Ϊ���������Ȼ����Ͷ���Ȼ�������ˮ�е��������ȥ���Ӷ�����ˮ�壬�Ȼ�����������
��������I�����ȸ���ͼ���жϷ�Ӧ����Ӧ���ĸ������ƶ����ĸ�����ķ�Ӧ���ʾʹ�
�ڵ���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯������ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
���ȼ���T1��ʱ�����ʵ����ʵ���Ũ�ȣ��ٸ���ƽ�ⳣ��K=
���㣻
��2��������Һ�������ȷ�����ӵ�ˮ��̶ȣ��ٸ��ݵ���غ�ȷ������Ũ�ȹ�ϵ��
��3���Ȼ�����ˮ�����������������壬������������ԣ������ܾ�ˮ��
�ڵ���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯������ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
���ȼ���T1��ʱ�����ʵ����ʵ���Ũ�ȣ��ٸ���ƽ�ⳣ��K=
| c2(SO3) |
| C2(SO2)��C(O2) |
��2��������Һ�������ȷ�����ӵ�ˮ��̶ȣ��ٸ��ݵ���غ�ȷ������Ũ�ȹ�ϵ��
��3���Ȼ�����ˮ�����������������壬������������ԣ������ܾ�ˮ��
����⣺��I���ٸ���ͼ��֪��a�����������¶ȣ���������������٣���Ӧ������Ӧ�����ƶ�����Ӧ���ĸ������ƶ����ĸ�����ķ�Ӧ���ʾʹ���������Ӧ���ʴ����淴Ӧ���ʣ��ʴ�Ϊ������
��a�����۷�Ӧ�Ƿ�ﵽƽ��״̬����λʱ��������1molO2��ͬʱ����2molS03�����Բ���ȷ���÷�Ӧ�Ƿ�ﵽƽ��״̬���ʴ���
b��������S02��O2��SO3��Ũ��֮��Ϊ2��1��2ʱ���÷�Ӧ���ܴﵽƽ��״̬��Ҳ����û�ﵽƽ��״̬�����뷴Ӧ��ij�ʼŨ�ȡ�ת�����йأ����Բ����ж��Ƿ�ﵽƽ��״̬���ʴ���
C���÷�Ӧ��һ�����������С�ķ�Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵĺ������䣬��������ѹǿ���ֲ��䣬������ƽ��÷�Ӧ�ﵽƽ��״̬������ȷ��
d���÷�Ӧ��һ�����������С�ķ�Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵ����ʵ������䣬���������ƽ����Է����������ֲ��䣬�������жϸ÷�Ӧ�ﵽƽ��״̬������ȷ��
��ѡcd��
�۸���ͼ��֪��T1��ʱ��������������1mol����μӷ�Ӧ��n��SO2��=��2-1��mol=1mol����μӷ�Ӧ��n��O2�����ڲμӷ�Ӧ��n��SO2����һ��Ϊ0.5mol������c��O2��=
=0.5mol/L��C��SO2��=
=0.5mol/L������������������Ͳμӷ�Ӧ�Ķ������������ͬ����Ϊ1mol������C��SO3��=
=0.5mol/L��ƽ�ⳣ��K=
=
=2L/mol���ʴ�Ϊ��2L/mol��
��2��̼��������������Σ�̼������Ӻ�笠����Ӷ���ˮ�⣬̼���ˮ��Һ�ʼ��ԣ���˵��̼�������ˮ��̶ȴ���笠����ӣ���Һ�ʵ����ԣ�����Һ�������������������ȣ����Ը��ݵ���غ�ã�c��NH4+��+c��H+��=2c��CO3 2- ��+c��HCO3-��+c��OH-�����ʴ�Ϊ��̼�������ˮ��̶ȴ���笠����ӣ�c��NH4+��+c��H+��=2c��CO3 2- ��+c��HCO3-��+c��OH-����
��3���Ȼ�����ǿ�������Σ���������ˮ�����������������壬������������ԣ�������ˮ������������ܾ�ˮ�������ӵ�ˮ�ⷴӦ����ʽΪ��Al 3++3H2O?Al��OH��3�����壩+3H+���ʴ�Ϊ��Al 3++3H2O?Al��OH��3�����壩+3H+��
��a�����۷�Ӧ�Ƿ�ﵽƽ��״̬����λʱ��������1molO2��ͬʱ����2molS03�����Բ���ȷ���÷�Ӧ�Ƿ�ﵽƽ��״̬���ʴ���
b��������S02��O2��SO3��Ũ��֮��Ϊ2��1��2ʱ���÷�Ӧ���ܴﵽƽ��״̬��Ҳ����û�ﵽƽ��״̬�����뷴Ӧ��ij�ʼŨ�ȡ�ת�����йأ����Բ����ж��Ƿ�ﵽƽ��״̬���ʴ���
C���÷�Ӧ��һ�����������С�ķ�Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵĺ������䣬��������ѹǿ���ֲ��䣬������ƽ��÷�Ӧ�ﵽƽ��״̬������ȷ��
d���÷�Ӧ��һ�����������С�ķ�Ӧ������Ӧ�ﵽƽ��״̬ʱ�������ʵ����ʵ������䣬���������ƽ����Է����������ֲ��䣬�������жϸ÷�Ӧ�ﵽƽ��״̬������ȷ��
��ѡcd��
�۸���ͼ��֪��T1��ʱ��������������1mol����μӷ�Ӧ��n��SO2��=��2-1��mol=1mol����μӷ�Ӧ��n��O2�����ڲμӷ�Ӧ��n��SO2����һ��Ϊ0.5mol������c��O2��=
| (1.5-0.5)mol |
| 2L |
| 1mol |
| 2L |
| 1mol |
| 2L |
| c2(SO3) |
| C2(SO2)��C(O2) |
| (0.5mol/L)2 |
| (0.5mol/L)2��(0.5mol/L) |
��2��̼��������������Σ�̼������Ӻ�笠����Ӷ���ˮ�⣬̼���ˮ��Һ�ʼ��ԣ���˵��̼�������ˮ��̶ȴ���笠����ӣ���Һ�ʵ����ԣ�����Һ�������������������ȣ����Ը��ݵ���غ�ã�c��NH4+��+c��H+��=2c��CO3 2- ��+c��HCO3-��+c��OH-�����ʴ�Ϊ��̼�������ˮ��̶ȴ���笠����ӣ�c��NH4+��+c��H+��=2c��CO3 2- ��+c��HCO3-��+c��OH-����
��3���Ȼ�����ǿ�������Σ���������ˮ�����������������壬������������ԣ�������ˮ������������ܾ�ˮ�������ӵ�ˮ�ⷴӦ����ʽΪ��Al 3++3H2O?Al��OH��3�����壩+3H+���ʴ�Ϊ��Al 3++3H2O?Al��OH��3�����壩+3H+��
������������ۺϣ��漰����ˮ�⡢ƽ�ⳣ���ļ��㡢ƽ��״̬���жϵ�֪ʶ�㣬ע��ƽ��״̬�ж�����ѡȡ���������DZ������ڷ�Ӧǰ��Ϊ�״��㣮

��ϰ��ϵ�д�
 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
�����Ŀ
 ��2010?Ϋ��һģ���о���ѧ��Ӧԭ���������������Ǻ�������ģ�
��2010?Ϋ��һģ���о���ѧ��Ӧԭ���������������Ǻ�������ģ�

 Fe��s��+CO2��g����
Fe��s��+CO2��g���� Fe��s��+CO2��g��
Fe��s��+CO2��g�� ��CO��= ��
��CO��= ��