题目内容
绿矾
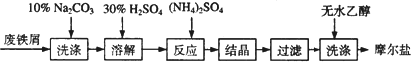
(FeSO4·7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体,反应原理为:(NH4)2SO4+FeSO4+6H2O![]() (NH4)2SO4·FeSO4·6H2O↓.
(NH4)2SO4·FeSO4·6H2O↓.
(1)
洗涤中Na2CO3的主要作用是________.(2)结晶过程中要加热蒸发溶剂,浓缩结晶.应加热到________时,停止加热.
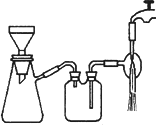
(3)过滤是用下图所示装置进行的,这种过滤跟普通过滤相比,除了过滤速度快外,还有一个优点是________.
(4)用无水乙醇洗涤的目的是________.
(5)产品中Fe2+的定量分析:制得的摩尔盐样品中往往含有极少量的Fe3+.为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性条件下KMnO4标准液滴定的方法.称取4
.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸.用0.2 mol/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液10.00 mL.①本实验的指示剂是________.(填字母)
A.酚酞
B.甲基橙
C.石蕊
D.不需要
②产品中Fe2+的质量分数为________.
解析:
|
(1)利用碳酸钠溶液呈碱性,除去铁表面的油污(2分) (2)加热到溶液表面出现晶膜时(2分) (3)得到较干燥的沉淀(2分) (4)除去水分,减少固体损失(2分) (5)①D(2分) ②14%(2分) |

 名校课堂系列答案
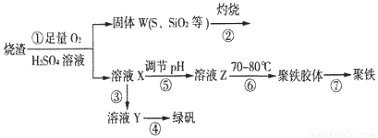
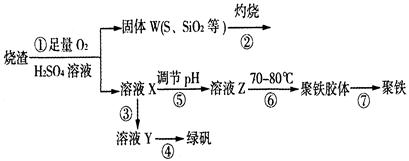
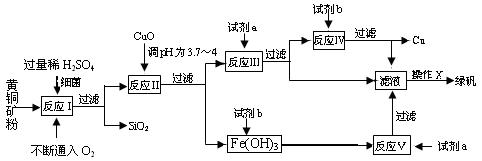
名校课堂系列答案(10分) 以黄铜矿(主要成份为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
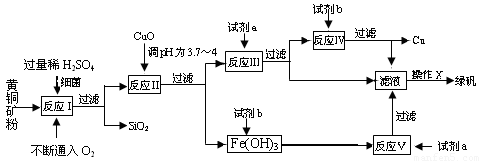
已知:①4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O;
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表:
|
沉淀物 |
Cu(OH)2 |
Fe(OH)3 |
Fe(OH)2 |
|
开始沉淀pH |
4.7 |
2.7 |
7.6 |
|
完全沉淀pH |
6.7 |
3.7 |
9.6 |
(1)试剂a是___________,试剂b是_____________。
(2)操作X应为蒸发浓缩、________________、________________。
(3)反应Ⅱ中加CuO调pH为3.7~4的目的是
。
(4)反应Ⅴ的离子方程式为___________________________。

 H如下表:
H如下表:
 中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。
中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。 加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。
加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。 量,一般采用在酸性下用KMnO4标准液滴定的方法。
量,一般采用在酸性下用KMnO4标准液滴定的方法。 (7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)
(7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)