题目内容
下列说法错误的是( )
| A、可用水鉴别苯、四氯化碳、乙醇三种无色液体 | B、取1 gNaOH固体于烧杯,加入9 mL水(ρ=1g?cm-3)充分搅拌配成10%的NaOH溶液 | C、用NaOH溶液就可鉴别K+、Mg2+、Al3+、Fe2+、Fe3+五种离子 | D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
分析:A.水与乙醇混溶,与四氯化碳混合分层后有机层在下层,与苯混合分层后有机层在上层;
B.溶质为1g,溶液为1g+9g=10g;
C.NaOH与K+、Mg2+、Al3+、Fe2+、Fe3+五种离子混合的现象分别为:无现象、白色沉淀、先出现白色沉淀后溶解、白色沉淀迅速变为灰绿色最后为红褐色、红褐色沉淀;
D.测定中和热,一般碱稍过量.
B.溶质为1g,溶液为1g+9g=10g;
C.NaOH与K+、Mg2+、Al3+、Fe2+、Fe3+五种离子混合的现象分别为:无现象、白色沉淀、先出现白色沉淀后溶解、白色沉淀迅速变为灰绿色最后为红褐色、红褐色沉淀;
D.测定中和热,一般碱稍过量.
解答:解:A.水与乙醇混溶,与四氯化碳混合分层后有机层在下层,与苯混合分层后有机层在上层,现象不同,可以鉴别,故A正确;
B.溶质为1g,溶液为1g+9g=10g,则溶质质量分数为
×100%=10%,故B正确;
C.NaOH与K+、Mg2+、Al3+、Fe2+、Fe3+五种离子混合的现象分别为:无现象、白色沉淀、先出现白色沉淀后溶解、白色沉淀迅速变为灰绿色最后为红褐色、红褐色沉淀,现象不同,可以鉴别,故C正确;
D.测定中和热,一般碱稍过量,保证酸完全反应,故D错误;
故选:D.
B.溶质为1g,溶液为1g+9g=10g,则溶质质量分数为
| 1g |
| 10g |
C.NaOH与K+、Mg2+、Al3+、Fe2+、Fe3+五种离子混合的现象分别为:无现象、白色沉淀、先出现白色沉淀后溶解、白色沉淀迅速变为灰绿色最后为红褐色、红褐色沉淀,现象不同,可以鉴别,故C正确;
D.测定中和热,一般碱稍过量,保证酸完全反应,故D错误;
故选:D.
点评:本题为小综合,涉及物质的鉴别、质量分数计算、中和热的测定等,侧重物质性质的考查,把握鉴别物质应利用不同现象来分析,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
下列说法错误的是( )
| A、C2H4和C4H8一定都能使溴水退色 | B、C2H6和C4H10一定是同系物 | C、C3H6不只表示一种物质 | D、烯烃中各同系物中碳的质量分数相同 |
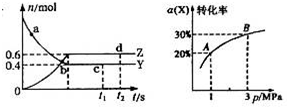 (2013?枣庄二模)一定温度下的密闭容器中发生反应:X(g)+3Y(g)f?2Z(g)△H<0,如图是反应达平衡及改变条件平衡移动的图象.下列说法错误的是( )
(2013?枣庄二模)一定温度下的密闭容器中发生反应:X(g)+3Y(g)f?2Z(g)△H<0,如图是反应达平衡及改变条件平衡移动的图象.下列说法错误的是( )