题目内容
某地环保部门取一定量某工厂所排废水试样分成甲、乙、丙、丁四份,进行如图所示探究.

已知废水试样中可能含有下表在的离子
请回答下列问题:
(1)离子X是 (填化学式,下同),离子Y是 .
(2)表中不能确定是否存在的阴离子是 ,能证明该阴离子是否存在的简单实验操作为 .
(3)写出废水试样中滴加淀粉一KI溶液所发生反应的离子方程式 :

已知废水试样中可能含有下表在的离子
| 离子 | |||||
| 阳离子 | Na+,Mg2+,X | ||||
| 阴离子 | Cl-,S
|
(1)离子X是
(2)表中不能确定是否存在的阴离子是
(3)写出废水试样中滴加淀粉一KI溶液所发生反应的离子方程式
分析:依据实验步骤分析判断,甲中加入溴水不褪色,证明不含还原性离子,推断不含SO32-;乙中加入酸化的氯化钡生成白色沉淀说明含有SO42-;丙中加入氢氧化钠溶液加热反应生成气体使湿润的红色石蕊试纸变蓝色,证明是氨气,说明原溶液中含有NH4+;丁中加入淀粉碘化钾溶液后溶液呈蓝色说明溶液中含有氧化性离子能氧化碘离子为单质碘;判断含有NO3-;
解答:解:依据实验步骤分析判断,甲中加入溴水不褪色,证明不含还原性离子,推断不含SO32-;乙中加入酸化的氯化钡生成白色沉淀说明含有SO42-;丙中加入氢氧化钠溶液加热反应生成气体使湿润的红色石蕊试纸变蓝色,证明是氨气,说明原溶液中含有NH4+;丁中加入淀粉碘化钾溶液后溶液呈蓝色说明溶液中含有氧化性离子能氧化碘离子为单质碘;判断含有NO3-;
(1)离子X为NH4+,离子Y为SO42-;故答案为:NH4+,SO42-;
(2)表中不能确定是否存在的阴离子是Cl-,能证明该阴离子是否存在的简单实验操作为,取少量溶液与试管中,加入稀硝酸,再加入硝酸银溶液生成白色沉淀证明氯离子的存在,故答案为:Cl-,取少量溶液与试管中,加入稀硝酸,再加入硝酸银溶液生成白色沉淀证明氯离子的存在;
(3)废水试样中滴加淀粉一KI溶液所发生反应的离子方程式:6I-+2NO3-+8H+=2NO↑+3I2+4H2O;
故答案为:6I-+2NO3-+8H+=2NO↑+3I2+4H2O;
(1)离子X为NH4+,离子Y为SO42-;故答案为:NH4+,SO42-;
(2)表中不能确定是否存在的阴离子是Cl-,能证明该阴离子是否存在的简单实验操作为,取少量溶液与试管中,加入稀硝酸,再加入硝酸银溶液生成白色沉淀证明氯离子的存在,故答案为:Cl-,取少量溶液与试管中,加入稀硝酸,再加入硝酸银溶液生成白色沉淀证明氯离子的存在;
(3)废水试样中滴加淀粉一KI溶液所发生反应的离子方程式:6I-+2NO3-+8H+=2NO↑+3I2+4H2O;
故答案为:6I-+2NO3-+8H+=2NO↑+3I2+4H2O;
点评:本题考查了离子检验的实验现象分析判断,离子共存分析,离子性质熟练掌握是解题关键,题目难度中等,

练习册系列答案
相关题目
某地环保部门取一定量某工厂所排废水试样分成甲、乙、丙、丁四份,进行如图所示探究.

已知废水试样中可能含有下表在的离子
| 离子 | |
| 阳离子 | Na+,Mg2+,X |
| 阴离子 | Cl-,S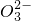 ,Y,N ,Y,N |
(1)离子X是______(填化学式,下同),离子Y是______.
(2)表中不能确定是否存在的阴离子是______,能证明该阴离子是否存在的简单实验操作为______.
(3)写出废水试样中滴加淀粉一KI溶液所发生反应的离子方程式______: