题目内容
17.下列关系正确的是( )| A. | 熔点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:溴苯>H2O>苯 | |
| C. | 含碳量:甲烷>乙烯>乙炔>苯 | |
| D. | 等物质的量燃烧耗O2量:己烷<环己烷<苯 |
分析 A.烷烃中,碳原子个数越多其熔沸点越高,同分异构体的烷烃,支链越多其熔沸点越低;
B.溴苯的密度大于1g/mL、水的密度是1g/mL、苯的密度小于1g/mL;
C.把其化学式都换算成碳原子个数相等的式子,H原子个数越多碳元素含量越低;
D.设烃的化学式为CxHy,1mol有机物CxHy完全燃烧耗氧量(x+$\frac{y}{4}$)mol判断.
解答 解:A.烷烃中,碳原子个数越多其熔沸点越高,同分异构体的烷烃,支链越多其熔沸点越低,所以熔点:2,2一二甲基戊烷>2,3一二甲基丁烷>戊烷>丙烷,故A错误;
B.溴苯的密度大于1g/mL、水的密度是1g/mL、苯的密度小于1g/mL,所以密度:溴苯>H2O>苯,故B正确;
C.甲烷、乙烯、乙炔、苯的最简式分别是CH4、CH2、CH、CH,这几种最简式中碳原子个数相等、H原子个数不等,H原子个数越多则C元素含量越低,所以含碳量:甲烷<乙烯<乙炔=苯,故C错误;
D.设烃的化学式为CxHy,1mol有机物CxHy完全燃烧耗氧量(x+$\frac{y}{4}$)mol,己烷、环己烷、苯的分子式分别是C6H14、C6H12、C6H6,碳原子个数相等H原子个数不等,H原子个数越多消耗氧气越多,所以等物质的量燃烧耗O2量:己烷>环己烷>苯,故D错误;
故选B.
点评 本题考查物质熔沸点高低判断、物质中元素含量判断、方程式的有关计算等知识点,侧重考查分析计算能力,注意CD中计算技巧,注意解题方法的积累及灵活运用,题目难度中等.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
8.能说明某烃分子里含有碳碳不饱和键的是( )
| A. | 分子组成中含碳氢原子个数比为1:2 | |
| B. | 能与溴发生加成反应而使溴水褪色,还能使酸性KMnO4溶液褪色 | |
| C. | 在空气中燃烧能产生黑烟 | |
| D. | 完全燃烧生成等物质的量的CO2和H2O |
12.关于铯(Cs)及其化合物的性质,说法正确的是( )
| A. | 金属铯的熔点比金属钠高 | B. | CsOH比NaOH的碱性强 | ||
| C. | Cs与H2O能剧烈反应,但没有钠剧烈 | D. | 碳酸铯难溶于水 |
2.下列组合中,中心离子的电荷数和配位数均相同的是( )
| A. | K[Ag(CN)2]、[Cu(NH3)4]SO4 | B. | [Ni(NH3)4]Cl2、[Ag(NH3)2]Cl | ||
| C. | [Ag(NH3)2]Cl、[Cu(NH3)2]Cl2 | D. | [Ni(NH3)4]Cl2、[Cu(NH3)4]SO4 |
9.下列变化需克服相同类型作用力的是( )
| A. | 碘和干冰的升华 | B. | 硅和冰的熔化 | ||
| C. | 氯化氢和氯化钾的溶解 | D. | 氯化钠和冰融化 |
6.下列表示物质结构的化学用语正确的是( )
| A. | 氯化氢的电子式: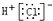 | B. | CO2的结构式:O=C=O | ||
| C. | 硫离子结构示意图: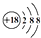 | D. | CCl4的电子式: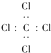 |