题目内容
2.下列说法正确的是( )| A. | π键是由两个p电子“头碰头”重叠形成的 | |
| B. | σ键是镜面对称,而π键是轴对称 | |
| C. | 乙烷分子中的键全为σ键而乙烯分子中含σ键和π键 | |
| D. | 含极性键的分子一定是极性分子 |
分析 σ键是“头碰头”重叠形成,可沿键轴自由旋转,为轴对称;而π键是由两个p电子“肩并肩”重叠形成,重叠程度小,为镜像对称,以此来解答.
解答 解:A.π键为p电子“肩并肩”重叠形成,而σ键为s或p电子“头碰头”重叠形成,故A错误;
B.σ键“头碰头”重叠为球对称,π键“肩并肩”重叠为镜面对称,故B错误;
C.乙烷分子中均为单键,乙烯中含C=C键,有1个π键,则乙烷分子中的键全为σ键而乙烯分子中含σ键和π键,故C正确;
D.CH4或CO2分子内含有极性键,但均为非极性分子,故D错误;
故选C.
点评 本题考查共价键的类型,明确σ键和π键的形成即可解答,题目难度不大,注重基础知识的考查.

练习册系列答案
相关题目
12.配制一定体积、一定物质的量浓度的溶液时,下列操作会使配得的溶液浓度偏大的是( )
| A. | 转移溶液时,没有洗涤玻璃棒和溶解用的烧杯 | |
| B. | 容量瓶中原有少量蒸馏水 | |
| C. | 定容时观察液面俯视 | |
| D. | 胶头滴管加水定容时,有少量水滴到容量瓶外 |
10.下列对分子中δ键重叠方式的分析不正确的是( )
| A | B | C | D |
| H2 | HCl | Cl2 | ClF |
| 两个原子的s轨道重叠 | 氢原子的s轨道和氯原子的p轨道重叠 | 一个氯原子的s轨道和另一个氯原子的p轨道重叠 | 氯原子的p轨道和氟原子的p轨道重叠 |
| A. | A | B. | B | C. | C | D. | D |
17.有机物(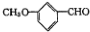 )有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )
)有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )
 )有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )
)有多种同分异构体,其中能与NaHCO3溶液反应且属于芳香族化合物的共有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.下列分子中,属于非极性分子的是( )
| A. | SO2 | B. | BeCl2 | C. | NF3 | D. | COCl2 |
14.在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是( )
| A. | 滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀 | |
| B. | 滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 | |
| C. | 测得反应后溶液中Na+与Cl-的个数比为1:1 | |
| D. | 滴入几滴酚酞试液,酚酞试液不变色 |
5. 表各组物质之间通过一步反应就能实现如图所示转化的是( )
表各组物质之间通过一步反应就能实现如图所示转化的是( )
 表各组物质之间通过一步反应就能实现如图所示转化的是( )
表各组物质之间通过一步反应就能实现如图所示转化的是( )| 物质选项 | a | b | c | m |
| A | N2 | NO | HNO3 | O2 |
| B | Na2CO 3 | NaHCO3 | NaOH | CO2 |
| C | H2S | S | SO2 | O2 |
| D | CH3CH2OH | CH3CHO | CH3COOH | O2 |
| A. | A | B. | B | C. | C | D. | D |