题目内容
14.在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是( )| A. | 滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀 | |
| B. | 滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 | |
| C. | 测得反应后溶液中Na+与Cl-的个数比为1:1 | |
| D. | 滴入几滴酚酞试液,酚酞试液不变色 |
分析 氢氧化钠与盐酸恰好完全反应生成氯化钠和水,反应后溶液呈中性,则c(H+)=c(OH-),根据电荷守恒可知c(Na+)=c(Cl-),即反应后溶液中Na+与Cl-的个数比为1:1;然后结合酚酞的表示范围、氯离子不参与反应等知识解答.
解答 解:A.由于加入了稀盐酸,溶液中存在Cl-,不论盐酸是过量还是恰好完全反应,Cl-会和Ag+生成沉淀,故A错误;
B.滴入适量FeCl3溶液,溶液变黄,但无沉淀生成.说明了盐酸是过量的.故B错误;
C.测得反应后溶液中Na+与Cl-的个数比为1:1,根据电荷守恒可知:c(H+)=c(OH-),证明氢氧化钠溶液和稀盐酸恰好完全反应,故C正确;
D.由于酚酞试液在酸性和中性条件下均不显色,则滴入几滴酚酞试液后不变色,不能证明二者恰好反应,故D错误;
故选C.
点评 本题考查酸碱中和反应实质及应用,题目难度不大,明确发生反应原理及恰好反应时特点为解答关键,注意掌握常见指示剂的不是范围及应用,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
4.下列物质性质排列顺序正确的是( )
①热稳定性:H2O>HF>H2S
②还原性:HI>HBr>HCl
③熔沸点:AsH3>PH3>NH3
④酸性:HNO3>H2CO3>H2SiO3.
①热稳定性:H2O>HF>H2S
②还原性:HI>HBr>HCl
③熔沸点:AsH3>PH3>NH3
④酸性:HNO3>H2CO3>H2SiO3.
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
5.利用辉铜矿冶铜时发生的主要反映为Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,下列有关该反应的说法中正确的是( )
| A. | 硫元素被氧化 | B. | O2失去电子 | ||
| C. | CuS仅作还原剂 | D. | 反应中Cu元素化合价没有发生变化 |
2.下列说法正确的是( )
| A. | π键是由两个p电子“头碰头”重叠形成的 | |
| B. | σ键是镜面对称,而π键是轴对称 | |
| C. | 乙烷分子中的键全为σ键而乙烯分子中含σ键和π键 | |
| D. | 含极性键的分子一定是极性分子 |
9.实验室有失去标签的三种化肥,已知可能是硫酸铵、氯化铵、硫酸钾.现各取少许进行鉴别,下列物质中能将上述肥料一次性区分开来的试剂是( )
| A. | 蒸馏水 | B. | 氢氧化钡溶液 | C. | 稀盐酸 | D. | 硝酸钡溶液 |
6.把a、b、c、d四块金属浸入稀硫酸中,用导线两两相连组成原电池,若a、b 相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡;b、d相连时,d极板溶解,则四种金属的活动性顺序为( )
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
3.有机物分子中原子或原子团之间的相互影响会导致化学性质不同.下列实验事实能证明此观点正确的是( )
| A. | 丙烯能发生加成反应,而丙烷不能发生加成反应 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| C. | 乙烯能使酸性高锰酸钾溶液褪色,而聚乙烯不能 | |
| D. | 烃类物质都能燃烧生成二氧化碳和水 |
17.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 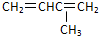 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. | CH3CH(OH)CH2CH32-羟基丁烷 | ||
| C. |  顺-2-丁烯 顺-2-丁烯 | D. | CH3CH(NH2)CH2COOH 3-氨基丁酸 |