题目内容
2.氮原子核外电子轨道表达式为( )| A. | 1s22s22p3 | B. |  | C. |  | D. |  |
分析 N原子核外有7个电子,分两层排布,根据原子核外电子排布原则:电子优先单独占据1个轨道,且自旋方向相同是,能量最低,由此分析解答.
解答 解:氮元素的原子核外有7个电子,轨道表示式为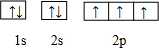 ,故选C.
,故选C.
点评 本题考查原子核外电子排布规律及轨道表达式的书写,题目难度不大,本题注意原子核外电子的排布和运动特点.

练习册系列答案
相关题目
19.下列解释事实或实验现象的化学用语正确的是( )
| A. | 将Cl2通入水中形成的溶液呈酸性 Cl2+H2O═2 H++Cl-+ClO- | |
| B. | 淀粉碘化钾溶液在空气中变蓝 4 I-+O2+2 H2O═2 I2+4 OH- | |
| C. | 钢铁表面的水膜酸性较强时,水膜中的H+会被还原 O2+4 H++4 e-═2 H2O | |
| D. | 向Na2SiO3溶液中通入过量SO2,有胶状物质生成SiO32-+SO2+H2O═H2SiO3↓+SO32- |
13.下列变化:①氮的固定(天然)②炽热的碳和浓硝酸反应 ③实验室制取氨气,按氮元素被氧化,被还原,既不被氧化也不被还原的顺序排列,正确的是( )
| A. | ③②① | B. | ②①③ | C. | ①②③ | D. | ③①② |
10.下列关于常见有机物的说法错误的是( )
| A. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯是发生取代反应 | |
| B. | C5H10不属于烷烃,C5H12属于烷烃且有三种同分异构体 | |
| C. | 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体 | |
| D. | 乙酸、葡萄糖在一定条件下均能与Cu(OH)2反应 |
17.常温下0.1mol/L氨水溶液的pH=a,下列能使溶液pH=(a-1)的措施是( )
| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的氯化铵固体 | ||
| C. | 加入等体积0.1 mol/L烧碱溶液 | D. | 加入等体积0.1 mol/L盐酸 |
14.物质的性质与其组成和结构相关,下列有关物质的物理性质比较错误的是( )
| A. | 硬度:白垩<金刚石 | B. | 熔点:Na<Mg | ||
| C. | 沸点:H2O<H2S | D. | 在水中溶解性:乙酸丁酯<乙酸 |
