题目内容
对于反应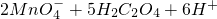 ═
═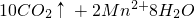 ,下列分析错误的是
,下列分析错误的是
- A.该反应氧化剂是H2C2O4
- B.反应中

- C.该反应的还原产物是Mn2+
- D.MnSO4可以作该反应的催化剂
A
分析:A.得电子化合价降低的反应物是氧化剂;
B.根据化合价的变化确定得到电子数;
C.氧化剂对应的产物是还原产物;
D.硫酸锰能加快反应速率,且没有强氧化性.
解答:A.该反应中,锰元素的化合价由+7价→+2价,所以高锰酸根离子得电子化合价降低作氧化剂,碳元素的化合价由+3价→+4价,所以草酸失电子化合价升高作还原剂,故A错误;
B.MnO4-→Mn 2+,一个高锰酸根离子失去5个电子生成锰离子,所以1mol高锰酸根离子得到5NA个电子,故B正确;
C.该反应中高锰酸根离子是氧化剂,则高锰酸根离子对应的锰离子是还原产物,故C正确;
D.硫酸锰能加快反应速率,且没有强氧化性,所以能作该反应的催化剂,故D正确;
故选A.
点评:本题考查了氧化还原反应,明确元素的化合价是解本题的关键,注意草酸中碳的平均化合价是+3价,为易错点.
分析:A.得电子化合价降低的反应物是氧化剂;
B.根据化合价的变化确定得到电子数;
C.氧化剂对应的产物是还原产物;
D.硫酸锰能加快反应速率,且没有强氧化性.
解答:A.该反应中,锰元素的化合价由+7价→+2价,所以高锰酸根离子得电子化合价降低作氧化剂,碳元素的化合价由+3价→+4价,所以草酸失电子化合价升高作还原剂,故A错误;
B.MnO4-→Mn 2+,一个高锰酸根离子失去5个电子生成锰离子,所以1mol高锰酸根离子得到5NA个电子,故B正确;
C.该反应中高锰酸根离子是氧化剂,则高锰酸根离子对应的锰离子是还原产物,故C正确;
D.硫酸锰能加快反应速率,且没有强氧化性,所以能作该反应的催化剂,故D正确;
故选A.
点评:本题考查了氧化还原反应,明确元素的化合价是解本题的关键,注意草酸中碳的平均化合价是+3价,为易错点.

练习册系列答案
相关题目
 对于可逆反应:2A(g)+B(g)?2C(g),分别测定反应在不同温度下达到平衡时B的转化率,绘制了如图所示的曲线,图中a、b、c三点分别表示不同的时刻状态.下列分析正确的是( )
对于可逆反应:2A(g)+B(g)?2C(g),分别测定反应在不同温度下达到平衡时B的转化率,绘制了如图所示的曲线,图中a、b、c三点分别表示不同的时刻状态.下列分析正确的是( )| A、该反应的△H<0 | B、b点时混合气体的平均摩尔质量不再变化 | C、增大压强,可使a点达到T1温度下平衡状态 | D、c点表示的状态:v(正)<v(逆) |
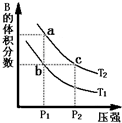 对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.
对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题. 乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.
乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.