题目内容
(1)按要求写出由第二周期元素为中心原子,通过sp3杂化形成物质的化学式:(各写一种)正四面体分子 ,三角锥形分子 ,V形分子 .
(2)写出下列原子的电子排布式:Cr
(3)画出下列原子的轨道表示式:C: .
(2)写出下列原子的电子排布式:Cr
(3)画出下列原子的轨道表示式:C:
考点:判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)由第二周期元素为中心原子,通过sp3杂化形成中性分子,说明中心原子价层电子对是4,如果是正四面体构型,则中心原子不含孤电子对,如果呈三角锥型结构说明中心原子含有一个孤电子对,如果呈V形结构则说明中心原子含有2个孤电子对;
(2)判断元素原子的核外电子数,先根据构造原理写出电子排布式,再写简易电子排布式;
(3)先根据构造原理写出电子排布式,再画出价电子轨道排布图.
(2)判断元素原子的核外电子数,先根据构造原理写出电子排布式,再写简易电子排布式;
(3)先根据构造原理写出电子排布式,再画出价电子轨道排布图.
解答:
解:(1)由第二周期元素为中心原子,通过sp3杂化形成中性分子,说明中心原子价层电子对是4,如果是正四面体构型,则中心原子不含孤电子对,如果呈三角锥型结构说明中心原子含有一个孤电子对,如果呈V形结构则说明中心原子含有2个孤电子对,所以正四面体分子为CH4或CF4,三角锥分子为 NH3或NF3,V形分子为为H2O,
故答案为:CH4或CF4;NH3或NF3;H2O;
(2)Cr元素为24号元素,原子核外有24个电子,其电子排布式为1s22s22p63s23p63d54s1,则简易电子排布式为[Ar]3d54s1,
故答案为:[Ar]3d54s1;
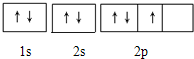
(3)C原子最外层4个电子,为2s22p2,两个电子分别占据2个p轨道,自旋反向相同,第一个电子层为1s2,其电子轨道表达式为: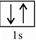
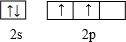 ,
,
故答案为:
 .
.
故答案为:CH4或CF4;NH3或NF3;H2O;
(2)Cr元素为24号元素,原子核外有24个电子,其电子排布式为1s22s22p63s23p63d54s1,则简易电子排布式为[Ar]3d54s1,
故答案为:[Ar]3d54s1;
(3)C原子最外层4个电子,为2s22p2,两个电子分别占据2个p轨道,自旋反向相同,第一个电子层为1s2,其电子轨道表达式为:

 ,
,故答案为:

 .
.
点评:本题考查了电子排布式和电子排布图、分子空间结构的判断等,题目侧重于基础知识的考查,难度不大,注意电子排布式和电子排布图的区别.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列设备工作时,将化学能转化为热能的是( )
| A | B | C | D |
 |  |  |  |
| 硅太阳能电池 | 锂离子电池 | 太阳能集热器 | 燃气灶 |
| A、A | B、B | C、C | D、D |
下列气体中,属于红棕色的是( )
| A、Cl2 |
| B、NH3 |
| C、NO2 |
| D、CO2 |
298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在该温度下取2mol N2和6mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量( )
| A、等于92.4 kJ |
| B、等于184.8 kJ |
| C、小于184.8 kJ |
| D、大于184.8 kJ |