题目内容
下列说法正确的是( )
| A、金属氧化物都是碱性氧化物 |
| B、由同种元素组成的物质一定是单质 |
| C、盐电离出的离子不一定有金属离子 |
| D、非金属氧化物都是酸性氧化物 |
考点:酸、碱、盐、氧化物的概念及其相互联系,单质和化合物
专题:物质的分类专题
分析:A、金属氧化物也可能是酸性氧化物或两性氧化物;
B、同种元素构成的纯净物属于单质;
C、盐是由金属阳离子(或铵根离子)和酸根离子构成的;
D、能和碱反应生成盐和水的氧化物属于酸性氧化物.
B、同种元素构成的纯净物属于单质;
C、盐是由金属阳离子(或铵根离子)和酸根离子构成的;
D、能和碱反应生成盐和水的氧化物属于酸性氧化物.
解答:
解:A、金属氧化物也可能是酸性氧化物或两性氧化物,如氧化铝属于两性氧化物,不是碱性氧化物,故A错误;
B、同种元素构成的纯净物属于单质,同种元素可以组成多种单质,如金刚石、石墨都是由碳元素构成的,二者在一起属于混合物,不是单质,故B错误;
C、盐是由金属阳离子(或铵根离子)和酸根离子构成的,所以盐电离出的离子不一定有金属离子,也可能是铵根离子,故C正确;
D、能和碱反应生成盐和水的氧化物属于酸性氧化物,非金属氧化物不一定是酸性氧化物,如CO属于不成盐氧化物,故D错误;
故选C.
B、同种元素构成的纯净物属于单质,同种元素可以组成多种单质,如金刚石、石墨都是由碳元素构成的,二者在一起属于混合物,不是单质,故B错误;
C、盐是由金属阳离子(或铵根离子)和酸根离子构成的,所以盐电离出的离子不一定有金属离子,也可能是铵根离子,故C正确;
D、能和碱反应生成盐和水的氧化物属于酸性氧化物,非金属氧化物不一定是酸性氧化物,如CO属于不成盐氧化物,故D错误;
故选C.
点评:本题考查了对单质、氧化物、盐的概念的理解,题目难度不大,注意把握相关概念是解决本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关说法正确的是( )
①进行中和热的测定实验时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度
②用滴定管量取盐酸前,先用蒸馏水洗净后再用待取盐酸进行润洗
③用蒸馏装置可以制乙酸乙酯,但温度计的水银球应放入液体中
④蔗糖水解实验,用NaOH中和稀硫酸之后再用新制的氢氧化铜检验是否水解.
①进行中和热的测定实验时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度
②用滴定管量取盐酸前,先用蒸馏水洗净后再用待取盐酸进行润洗
③用蒸馏装置可以制乙酸乙酯,但温度计的水银球应放入液体中
④蔗糖水解实验,用NaOH中和稀硫酸之后再用新制的氢氧化铜检验是否水解.
| A、②③ | B、①③ | C、①②④ | D、①② |
下列物质中,形成的化学键是离子键的是( )
| A、KCl |
| B、NH3 |
| C、CO2 |
| D、C12 |
室温下,下列各组离子在指定溶液中能大量共存的是( )
| A、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| B、加入甲基橙试液呈红色的溶液:NH4+,K+,SO42-,Cl- |
| C、Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
| D、pH=12的溶液中:NO3-、I-、Na+、Al3+ |
下列化学实验事实及解释都正确的是( )
| A、碳酸钙不溶于水,所以它是非电解质 |
| B、强电解质的水溶液一定比弱电解质溶液的导电能力强 |
| C、升高温度可以增大单位体积内活化分子的百分数 |
| D、非自发反应在任何条件下都不能实现 |
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为aHClO3→bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色.下列说法正确的是( )
| A、由反应可确定:氧化性HClO4>HClO3 |
| B、变蓝的淀粉碘化钾试纸褪色,可能发生:5Cl2+I2+6H2O→12H++10Cl-+2IO3- |
| C、若氯酸分解所得混合气体,lmol该混合气体质量为47.6g,则反应方程式可表示为:26HClO3→15O2↑+8Cl2↑+10HClO4+8H2O |
| D、若化学计量数a=8、b=3,则该反应转移电子数为12e |
下列有关环境问题都是由化学物质引起的,在下列组合中对应的化合物不正确的是( )
| A、白色污染:废弃塑料 |
| B、光化学烟雾:二氧化氮? |
| C、臭氧层破坏:氟氯烃? |
| D、温室效应:二氧化硫 |
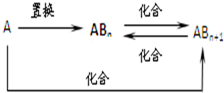 元素A的单质及元素A与元素B形成的化合物有如图所示的转化关系:
元素A的单质及元素A与元素B形成的化合物有如图所示的转化关系: