题目内容
下列物质中,形成的化学键是离子键的是( )
| A、KCl |
| B、NH3 |
| C、CO2 |
| D、C12 |
考点:离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,部分碱、大多数盐、金属氧化物中都含有离子键.
解答:
解:A.KCl中钾离子和氯离子之间存在离子键,故A正确;
B.氨气分子中N原子和H原子之间存在共价键,故B错误;
C.二氧化碳分子中C原子和O原子之间存在共价键,故C错误;
D.氯气分子中两个氯原子之间存在共价键,故D错误;
故选A.
B.氨气分子中N原子和H原子之间存在共价键,故B错误;
C.二氧化碳分子中C原子和O原子之间存在共价键,故C错误;
D.氯气分子中两个氯原子之间存在共价键,故D错误;
故选A.
点评:本题考查了离子键和共价键的判断,明确二者概念是解本题关键,注意不能根据是否含有金属元素判断离子键,如铵盐全部是由非金属元素组成的,但含有离子键,氯化铝中含有金属元素但只含共价键,为易错点.

练习册系列答案
相关题目
下列各组物质中,所含分子数相同的是( )
| A、9 g H2O和0.5molBr2 |
| B、5.6LN2(标准状态)和11 g CO2 |
| C、10 g H2和10 g O2 |
| D、224mlH2(标准状态) 和0.1molN2 |
下列说法正确的是( )
| A、金属氧化物都是碱性氧化物 |
| B、由同种元素组成的物质一定是单质 |
| C、盐电离出的离子不一定有金属离子 |
| D、非金属氧化物都是酸性氧化物 |
1.52g铜镁合金完全溶解于50mL密度为1.40g/cm3、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol?L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A、该合金中铜与镁的物质的量之比是2:1 |
| B、该浓硝酸中HNO3的物质的量浓度是14.0 mol?L-1 |
| C、NO2和N2O4 的混合气体中,NO2和N2O4 的物质的量之比是1:4 |
| D、得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL |
下列属于同分异构体的组合是( )
| A、戊烷与乙烷 |
| B、淀粉和纤维素 |
C、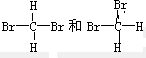 |
| D、CH3CH2CH2CH3和CH3CH(CH3)2 |
检验乙醇中混有的水应用下列哪种试剂( )
| A、金属钠 | B、浓硫酸 |
| C、无水硫酸铜 | D、生石灰 |