题目内容
16.下列有关金属及其化合物的说法正确的是( )| A. | Mg和Al都可以用电解法冶炼得到 | |
| B. | Mg和Fe在一定条件下与水反应都生成H2 和对应的碱 | |
| C. | Fe和Cu常温下放入浓硝酸中发生的现象相同 | |
| D. | Na2O和Na2O2与CO2反应产物也相同 |
分析 A.Mg和Al都为活泼金属,应用电解法冶炼;
B.铁和水蒸气在高温下反应生成四氧化三铁;
C.Cu常温下与浓硝酸反应,Fe常温下在浓硝酸中钝化;
D.Na2O和CO2反应生成碳酸钠,Na2O2与CO2反应生成碳酸钠和氧气.
解答 解:A.常见金属的冶炼方法有电解法、热还原法、热分解法等,其中Mg和Al都为活泼金属,应用电解法冶炼,故A正确;
B.铁和水蒸气在高温下反应生成四氧化三铁,不生成碱,故B错误;
C.Cu常温下与浓硝酸反应生成二氧化氮,Fe常温下在浓硝酸中钝化,故C错误;
D.Na2O和CO2反应生成碳酸钠,Na2O2与CO2反应除生成碳酸钠外,还有氧气,故D错误.
故选:A.
点评 本题考查较为综合,涉及钠、镁、铝、铁等金属单质及其化合物的性质,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,为高频考点,注相关基础知识的积累,难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
7.某实验小组用NaOH标准溶液测定盐酸溶液的物质的量浓度,其部分操作步骤如下:
(1)用酸式滴定管量取25.00mL待测液于锥形瓶中,并滴加几滴酚酞作指示剂.
(2)用0.2500mol•L-1标准NaOH溶液滴定待测盐酸溶液,滴定时左手挤压碱式滴定管的玻璃球,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色(从“滴定管内液面”、“锥形瓶内溶液颜色”中选择填空)的变化,直到滴定终点,滴定终点时锥形瓶内溶液的pH约为8.2,达到终点的具体现象是由无色变为浅红色,且半分钟不变色.
(3)若两次实验滴定的数据如表:
根据表数据,计算出的待测盐酸溶液的物质的量浓度是0.20mol•L-1.
(4)问题讨论:若碱式滴定管下端尖嘴中有气泡存在,除去的方法是弯曲乳胶管,让尖嘴略朝上,挤捏乳胶管.
(5)误差分析:若其它操作均正确,出现下列情形时,可能导致测定结果有偏差.
①滴定时,滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,测定结果将偏高(填偏高、偏低或无影响,下同).
②读数时,滴定前仰视,滴定毕俯视,测定结果将偏低.
(1)用酸式滴定管量取25.00mL待测液于锥形瓶中,并滴加几滴酚酞作指示剂.
(2)用0.2500mol•L-1标准NaOH溶液滴定待测盐酸溶液,滴定时左手挤压碱式滴定管的玻璃球,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色(从“滴定管内液面”、“锥形瓶内溶液颜色”中选择填空)的变化,直到滴定终点,滴定终点时锥形瓶内溶液的pH约为8.2,达到终点的具体现象是由无色变为浅红色,且半分钟不变色.
(3)若两次实验滴定的数据如表:
| 滴定次数 | 待测液体积(mL) | 标准NaOH溶液体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 10.80 | 30.70 |
| 第二次 | 25.00 | 14.20 | 34.30 |
(4)问题讨论:若碱式滴定管下端尖嘴中有气泡存在,除去的方法是弯曲乳胶管,让尖嘴略朝上,挤捏乳胶管.
(5)误差分析:若其它操作均正确,出现下列情形时,可能导致测定结果有偏差.
①滴定时,滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,测定结果将偏高(填偏高、偏低或无影响,下同).
②读数时,滴定前仰视,滴定毕俯视,测定结果将偏低.
11.下列反应属于吸热反应的是( )
| A. | C6H12O6(葡萄糖)+6O2═6CO2+6H2O | B. | CH3COOH+KOH═CH3COOK+H2O | ||
| C. | 所有高温条件下发生的反应 | D. | C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO |
6.酚酞是中学化学中常用的酸碱指示剂,其结构如图,其含有的饱和碳原子个数为( )
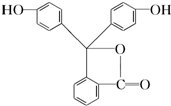

| A. | 1 | B. | 2 | C. | 3 | D. | 5 |