题目内容
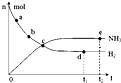 科学家一直致力于“人工固氮”的新方法研究.目前合成氨技术原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1.在673K,30MPa下,上述合成氨反应中n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
科学家一直致力于“人工固氮”的新方法研究.目前合成氨技术原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ?mol-1.在673K,30MPa下,上述合成氨反应中n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A、点a的正反应速率比点b的大 |
| B、点c处反应达到化学平衡状态 |
| C、点d和点e处的n(N2)不相同 |
| D、点e反应达到化学平衡状态,反应停止 |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A.浓度越大反应速率越快;
B.a、b、c之后氢气的物质的量继续变化,未达到平衡,反应向正反进行;
C.d、e对应氢气、氨气的物质的量不变,处于平衡状态;
D.d、e对应氢气、氨气的物质的量不变,处于平衡状态是动态平衡.
B.a、b、c之后氢气的物质的量继续变化,未达到平衡,反应向正反进行;
C.d、e对应氢气、氨气的物质的量不变,处于平衡状态;
D.d、e对应氢气、氨气的物质的量不变,处于平衡状态是动态平衡.
解答:
解:A.a点反应物的浓度大于b点,浓度越大反应速率越快,故a点反应速率更大,故A正确;
B.点c之后氢气的物质的量继续减小,未达到平衡,反应向正反进行,故B错误;
C.d、e对应氢气、氨气的物质的量不变,处于平衡状态,点d和点e处的n (N2)相同,故C错误;
D.d、e对应氢气、氨气的物质的量不变,处于平衡状态,平衡时动态平衡丙未停止,故D错误;
故选A.
B.点c之后氢气的物质的量继续减小,未达到平衡,反应向正反进行,故B错误;
C.d、e对应氢气、氨气的物质的量不变,处于平衡状态,点d和点e处的n (N2)相同,故C错误;
D.d、e对应氢气、氨气的物质的量不变,处于平衡状态,平衡时动态平衡丙未停止,故D错误;
故选A.
点评:本题考查了化学平衡影响因素分析,注意图象变化的分析判断,掌握平衡调整和移动原理是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如图是电解溶液CuCl2的装置,其中c、d为石墨电极,则下列有关判断正确的是( )


| A、a为正极、d为阴极 |
| B、c电极发生还原反应 |
| C、电解过程中,d电极质量增加 |
| D、电解过程中,氯离子浓度不变 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 0.1mol?L-1的氨水中含有的NH3?H2O分子数为0.1NA |
| B、电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA |
| C、标准状况下,2.24L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D、一定条件下,4.6g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
在氢氧化钠的溶液中能大量共存且溶液为无色的一组离子是( )
| A、K+、HCO3-、Cl-、SO42- |
| B、S2-、CO32-、CH3COO-、K+ |
| C、K+、Mg2+、SO42-、Na+ |
| D、Na+、MnO4-、NO3-、SO42- |
 用酸性氢氧燃料电池为电源电解CuSO4溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )
用酸性氢氧燃料电池为电源电解CuSO4溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )| A、燃料电池工作时,负极反应为O2+4H++4e-═2H2O |
| B、a极是石墨,b极是铜时,b极的电极反应为:4OH--4e-═2H2O+O2↑ |
| C、a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为224ml(标准状况),则原溶液的浓度是0.1mol/L |
| D、a、b两极均是石墨时,若a极产生的气体为56mL(标准状况),则U形管中溶液的PH为2(体积变化忽略不计) |
下列方法正确的是( )
A、[SiO4]的四面体结构: |
| B、C2H5Cl与NaOH溶液混合加热水解后,加入AgNO3溶液,以检验Cl- |
| C、在MgCl2晶体中含有共价键和离子键 |
| D、0.5g C3H4中含有共用电子对的数目为1×6.02×1023 |
下列实验能达到预期目的是( )
①用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子;
②用溴水检验汽油中是否含有不饱和链烃;
③用乙醇从碘水中萃取碘;
④用盐析方法分离提纯蛋白质;
⑤用加热方法提纯含有少量碳酸氢钠的碳酸钠固体;
⑥闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔.
①用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子;
②用溴水检验汽油中是否含有不饱和链烃;
③用乙醇从碘水中萃取碘;
④用盐析方法分离提纯蛋白质;
⑤用加热方法提纯含有少量碳酸氢钠的碳酸钠固体;
⑥闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔.
| A、②④⑤⑥ | B、①③⑥ |
| C、①②④⑤⑥ | D、②③④⑤ |
在通常条件下,下列各组物质的性质排列正确的是( )
| A、水溶性:NH3>H2S>I2 |
| B、沸点:HF>HCl>HBr |
| C、硬度:金刚石>晶体硅>碳化硅 |
| D、熔点:LiF>KF>NaF |