题目内容
下列电离方程式书写正确的是( )
| A、H2SO4=H2++SO42-- |
| B、MgCl 2=Mg2++Cl2- |
| C、NaNO3=Na++NO3- |
| D、NaHSO4=Na++HSO4- |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式.离子所带电荷数一般可根据它们在化合物中的化合价来判断.所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等.
解答:
解:A、硫酸水溶液中完全电离出氢离子和硫酸根离子,H2SO4=2H++SO42-,故A错误;
B、氯化镁是强电解质电离生成氯离子和镁离子,MgCl2=Mg2++2Cl-,故B错误;
C、硝酸钠是盐属于强电解质,完全电离为钠离子和硝酸根离子,NaNO3=Na++NO3-,故C正确;
D、硫酸氢钠水溶液中完全电离生成钠离子、氢离子、硫酸根离子,NaHSO4=Na++H++SO4-,故D错误;
故选C.
B、氯化镁是强电解质电离生成氯离子和镁离子,MgCl2=Mg2++2Cl-,故B错误;
C、硝酸钠是盐属于强电解质,完全电离为钠离子和硝酸根离子,NaNO3=Na++NO3-,故C正确;
D、硫酸氢钠水溶液中完全电离生成钠离子、氢离子、硫酸根离子,NaHSO4=Na++H++SO4-,故D错误;
故选C.
点评:本题考查了电解质电离分析判断,掌握正确书写电离方程式的方法,并会正确判断离子方程式的正误.

练习册系列答案
相关题目
有关电解质的说法正确的是( )
| A、FeCl3溶液能够导电,所以FeCl3溶液是电解质 |
| B、CO2水溶液能够导电,所以CO2是电解质 |
| C、液态的铜导电性很好,所以铜是电解质 |
| D、NaOH固体溶于水后能导电,所以NaOH是电解质 |
下列各图所表示的反应是吸热反应的是( )
A、 反应过程 |
B、 反应过程 |
C、 反应过程 |
D、 反应过程 |
下列分子中各原子都满足8电子稳定结构的化合物( )
| A、CH4 |
| B、CH2=CH2 |
| C、CO2 |
| D、N2 |
下列说法中正确的是( )
| A、2mol CH4的质量和O2的摩尔质量都是32g |
| B、1mol任何气体中都含有相同的原子数 |
| C、0.5molNaCl约含有6.02×1023个离子 |
| D、1mol/LKCl溶液中含有溶质1mol |
下列有关化学用语使用正确的是( )
A、CH4分子的比例模型: |
| B、乙醇的分子式CH3CH2OH |
| C、苯的最简式 C6H6 |
| D、乙烯的结构简式CH2CH2 |
设NA为阿伏加德罗常数,下列有关说法正确的是( )
| A、0.5mol苯分子中含有C=C双键数为1.5NA | ||
| B、2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | ||
C、标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为
| ||
| D、1 mol甲基(-CH3)所含的电子总数为8 NA |
下列有机反应的化学方程式和反应类型均正确的是( )
A、CH4+Cl2
| ||
B、nCH3-CH=CH2
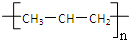 聚合反应 聚合反应 | ||
C、淀粉:(C6H10O5)n+nH2O
| ||
D、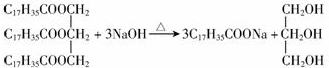 皂化反应 皂化反应 |