题目内容
(15分)工业上研究燃料脱硫的过程中,涉及如下反应:
CaSO4(s)+CO(g)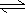 CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
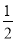 CaSO4(s)+2CO(g)
CaSO4(s)+2CO(g)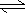
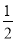 CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
(1)反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H= ;平衡常数K=____ (用K1,K2表示)。
CaS(s)+3CO2(g)的△H= ;平衡常数K=____ (用K1,K2表示)。
(2)某温度下在一密闭容器中若只发生反应I,测得数据如下:

前100 s 内v(SO2)= mo1·L-1·s-l,平衡时CO的转化率为 。
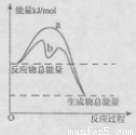
(3)若只研究反应II,在不同条件下其反应能量变化如下图所示:图中曲线a到曲线b的措施是________,恒温恒容时,下列说法能说明反应Ⅱ到达平衡状态的是____ 。
A.体系中气体的平均摩尔质量不再改变
B.v(CO)=v(CO2)
C.CO的转化率达到了最大限度
D.体系内气体压强不再发生变化
(4)某科研小组研究在其它条件不变的情况下,改变起始一氧化碳物质的量[用n(CO)表示]对CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):
CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):

①比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是
____ 。
②图像中T2 T1(填“高于”、“低于”、“等于”或“无法确定”):判断的
理由是____ 。
(1)-394kJ/mol (2分) 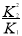 (2分);(2)0.009(1分) 60%(2分);
(2分);(2)0.009(1分) 60%(2分);
(3)使用催化剂(1分),A、C(2分)
(4)① c (2分)②低于(1分) 该反应为放热反应,升高温度平衡向逆反应方向移动,CO2体积分数降低,故T2低于T1(2分)
【解析】
试题分析:(1)II×2-I整理可得:CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H=-394kJ/mol; K1=
CaS(s)+3CO2(g)的△H=-394kJ/mol; K1=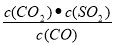 ; K2=
; K2=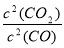 ;K=
;K=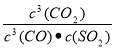 ;所以K=
;所以K=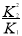 。(2)在反应I中,前100 s 内v(CO)=(2-1.1)mol/L÷100s=0.009mol/(L·s),v(SO2)== v(CO)=0.009mol/(L·s);平衡时CO的转化率为[(2-0.8)÷2]×100%=60%;(3)若只研究反应II,在不同条件下其反应能量变化如图所示,由于降低了反应的活化能,反应热没有变化,所以图中曲线a到曲线b的措施是加入了催化剂;A.由于反应前后气体的质量发生了变化,而气体的物质的量不变,所以若体系中气体的平均摩尔质量不再改变,则气体的质量不再发生变化,反应达到平衡状态,正确;B.因为在方程式是两种气体的方程式的系数相同,所以在任何时刻都存在v(CO)=v(CO2),因此不能作为判断反应达到平衡的标志,错误;C.反应物CO达到平衡时其的转化率达到了最大限度,正确;D.由于容器的容积不变,反应前后气体的体积相等,所以在任何时刻都存在体系内气体压强不再发生变化,故不能作为判断反应达到平衡状态的标志,错误;(4)①根据图像可知a、b、c三点同一温度下不同的n(CO)开始投入量的所处的平衡状态中,由于CO越大,c(CO)就越大,增大反应物的浓度,可以提高其它反应物的转化率,所以这三点中反应物SO2的转化率最高的是c点;②由于反应CaO(s)+3CO(g)+SO2(g)
。(2)在反应I中,前100 s 内v(CO)=(2-1.1)mol/L÷100s=0.009mol/(L·s),v(SO2)== v(CO)=0.009mol/(L·s);平衡时CO的转化率为[(2-0.8)÷2]×100%=60%;(3)若只研究反应II,在不同条件下其反应能量变化如图所示,由于降低了反应的活化能,反应热没有变化,所以图中曲线a到曲线b的措施是加入了催化剂;A.由于反应前后气体的质量发生了变化,而气体的物质的量不变,所以若体系中气体的平均摩尔质量不再改变,则气体的质量不再发生变化,反应达到平衡状态,正确;B.因为在方程式是两种气体的方程式的系数相同,所以在任何时刻都存在v(CO)=v(CO2),因此不能作为判断反应达到平衡的标志,错误;C.反应物CO达到平衡时其的转化率达到了最大限度,正确;D.由于容器的容积不变,反应前后气体的体积相等,所以在任何时刻都存在体系内气体压强不再发生变化,故不能作为判断反应达到平衡状态的标志,错误;(4)①根据图像可知a、b、c三点同一温度下不同的n(CO)开始投入量的所处的平衡状态中,由于CO越大,c(CO)就越大,增大反应物的浓度,可以提高其它反应物的转化率,所以这三点中反应物SO2的转化率最高的是c点;②由于反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H=-394kJ/mol,即该反应是放热反应,升高温度,平衡向逆反应方向移动,CO2体积分数降低,故T2低于T1。
CaS(s)+3CO2(g)的△H=-394kJ/mol,即该反应是放热反应,升高温度,平衡向逆反应方向移动,CO2体积分数降低,故T2低于T1。
考点:考查盖斯定律的应用、化学平衡常数的表达与比较、化学平衡状态的判断、不同反温度的比较化学反应速率和物质平衡转化率的计算的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
A.X、Y元素的金属性 X<Y
B.一定条件下, Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
下列实验方案中,不能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |
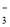 、Al3+、Cl-
、Al3+、Cl-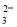 、Ca2+、NO
、Ca2+、NO 、Cl-、Cu2+
、Cl-、Cu2+
 2C
2C