题目内容
19. 一定温度下,在一容积不变的容器中,发生化学反应aA(g)+bB(g)═cC(g),采用不同比例的A,B作为起始物,测量反应达平衡时A和B的转化率,得到如图图象:
一定温度下,在一容积不变的容器中,发生化学反应aA(g)+bB(g)═cC(g),采用不同比例的A,B作为起始物,测量反应达平衡时A和B的转化率,得到如图图象:(1)图象中X表示B的转化率;
(2)向容积为2L的密闭容器中充入2mol A和2mol B,4min后反应达平衡,测得A的转化率为60%,则B的转化率为20%,若C的反应速率为0.1mol•L-1•min-1,则a,b,c的值分别为3,1,2;
(3)若在此容器中,按照n(A):n(B)=a:b的比例加入一定量的A和B,平衡后将其中的C移出一部分,当再次达到平衡时,C的体积分数减小(填“增大”、“减小”或“不变”,下同),若容器为一体积可变、压强不变的容器,同样加入A,B,达平衡后,移出一部分C,再次达到平衡时,C的体积分数不变.
分析 (1)随$\frac{n(A)}{n(B)}$增大,可以看作B为定量,增大A的物质的量,则A的转化率减小,B的转化率增大;
(2)由图可知,当$\frac{n(A)}{n(B)}$=3时A、B的转化率相等,则a:b=3:1,根据A的转化率计算参加反应的A的物质的量,再根据化学计量数之比计算参加反应B的物质的量,可计算B的转化率;
计算生成C的物质的量,物质的量之比等于化学计量数之比;
(3)若在此容器中,按照n(A):n(B)=a:b的比例加入一定量的A和B,平衡后将其中的C移出一部分,当再次达到平衡时,等效为降低压强;
若容器为一体积可变、压强不变的容器,同样加入A,B,达平衡后,移出一部分C,完全转化到左边A、B的物质的量之比仍为a:b,再次达到平衡时与原平衡为等效平衡.
解答 解:(1)随$\frac{n(A)}{n(B)}$增大,可以看作B为定量,增大A的物质的量,则A的转化率减小,B的转化率增大,由图可知,X表示B的转化率,Y表示A的转化率,
故答案为:B;
(2)由图可知,当$\frac{n(A)}{n(B)}$=3时A、B的转化率相等,则a:b=3:1,参加反应的A的物质的量为2mol×60%=1.2mol,则参加反应B的物质的量为1.2mol×$\frac{1}{3}$=0.4mol,故B的转化率为$\frac{0.4mol}{2mol}$×100%=20%;
生成C的物质的量为0.1mol•L-1•min-1×4min×2L=0.8mol,物质的量之比等于化学计量数之比,则a:b:c=1.2mol:0.4mol:0.8mol=3:1:2,
故答案为:20%;3,1,2;
(3)发生化学反应:3A(g)+B(g)═2C(g),若在此容器中,按照n(A):n(B)=a:b的比例加入一定量的A和B,平衡后将其中的C移出一部分,等效为在原平衡的基础上降低压强,平衡向逆反应方向移动,平衡时C的体积分数减小;
若容器为一体积可变、压强不变的容器,同样加入A,B,达平衡后,移出一部分C,完全转化到左边A、B的物质的量之比仍为a:b,故为等效平衡,平衡时C的体积分数不变,
故答案为:减小;不变.
点评 本题考查化学平衡计算、等效平衡,(2)中关键是根据图中转化率相等确定a与b的关系,(3)中注意理解等效平衡规律,难度中等.

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案| A. | 升高温度,固体的量减少 | |
| B. | 加入少量Na2CO3粉末能增大钙离子的浓度 | |
| C. | 恒温下加入少量CaO,溶液的pH增大 | |
| D. | 降低温度,溶液中c(OH-)增大 |
| A. | 0mol | B. | 1mol | C. | 2mol | D. | 3mol |
| A. | 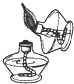 点燃酒精灯 | B. | 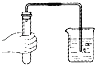 检验气密性 | C. | 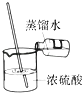 稀释浓硫酸 | D. | 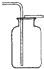 收集氢气. |
| A. | 蒸发使用的主要仪器是蒸发皿、酒精灯、玻璃棒、带铁圈的铁架台 | |
| B. | 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 | |
| C. | 丁达尔效应可以鉴别胶体和溶液 | |
| D. | 用规格为10 mL的量筒量取6.20 mL的液体 |
