题目内容
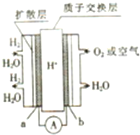 某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )
某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )| A、a极为该电池的负极 |
| B、该电池的正极反应式为O2+4e-+2H2O=4OH- |
| C、多孔活性铂电极有利于吸附气体,增大接触面积 |
| D、H+(质子)由负极移向正极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该电池属于酸性氢氧燃料电池,电池工作时的正负极反应式分别为:正极:O2+4H++4e-═2H2O;负极:H2-2e-═2H+,在原电池中阳离子向电池的正极移动,阴离子向电池的负极移动,以此解答该题.
解答:
解:A.a极通入氢气,发生氧化反应,是原电池的负极,故A正确;
B.通入氧气的一极是原电池的正极,在酸性条件下,氧气得电子被还原,发生的电极反应为:O2+4H++4e-═2H2O,故B错误;
C.多孔活性铂电极具有较强的吸附性,有利于吸附气体,增大接触面积,故C正确;
D.阳离子向正极移动,故D正确.
故选B.
B.通入氧气的一极是原电池的正极,在酸性条件下,氧气得电子被还原,发生的电极反应为:O2+4H++4e-═2H2O,故B错误;
C.多孔活性铂电极具有较强的吸附性,有利于吸附气体,增大接触面积,故C正确;
D.阳离子向正极移动,故D正确.
故选B.
点评:本题考查了原电池原理,为高频考点,明确燃料电池中得失电子的物质即可解答,注意该原电池是酸性电池,可能很多同学不能根据“质子交换膜”确定溶液的酸碱性,为易错点.

练习册系列答案
相关题目
下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
| A、在常温常压下,16g O2和O3的混合气体所含原子数目为NA |
| B、1mol/L K2SO4溶液所含K+数目为2NA |
| C、在标准状况下,22.4L水所含分子数目为NA |
| D、0.1mol Fe与足量稀盐酸完全反应时,转移电子数目为0.3NA |
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两电极,通过导线与直流电源相连.下列说法不正确的是( )
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两电极,通过导线与直流电源相连.下列说法不正确的是( )| A、若电镀铜,则Y为铜电极,电解液a可以是硫酸铜或氯化铜溶液 |
| B、若X为铁电极,Y为石墨电极,电解饱和氯化钠溶液一段时间,在两极分别滴加酚酞,X极变红色 |
| C、若X为铂电极,Y为铜电极,a溶液为稀硫酸,经过一段时间后,X极可能析出红色固体 |
| D、若精炼铜,则X用粗铜,Y用精铜 |
下列说法正确的是( )
| A、凡是没有单质参加的化合反应一定是非氧化还原反应 |
| B、有单质参加的反应一定是氧化还原反应 |
| C、凡是有盐参加的反应都是复分解反应 |
| D、置换反应一定是氧化还原反应 |
下列物质中含原子数最多的是( )
| A、6.4g O2 |
| B、8.8g CO2 |
| C、0.1mol N2 |
| D、3.01×1022个H2O |
下列说法正确的是( )
| A、元素的单质可由氧化或还原含该元素的化合物来制得 |
| B、得电子越多的氧化剂,其氧化性就越强 |
| C、金属氧化物一定是碱性氧化物 |
| D、凡在溶液中能电离出H+的化合物都属于酸 |
下列物质所配成的0.1mol/L溶液中,离子浓度由大到小顺序排列正确的( )
| A、NH4Cl:(Cl-)>(H+)>(NH4+)>(OH-) |
| B、Na2CO3:(Na+)>(CO32-)>(HCO3-)>(OH-)>(H+) |
| C、NaHCO3:(Na+)>(CO32-)>(HCO3-)>(OH-)>(H+) |
| D、(NH4)2SO4:(NH4+)>(SO42-)>(H+)>(OH-) |
几种短周期元素的原子半径及主要化合价如表( )
下列叙述错误的是(其中NA表示阿伏加德罗常数的值)
| 元素代号 | X | Y | Z | M | N | P |
| 原子半径/nm | 0.186 | 0.143 | 0.075 | 0.074 | 0.152 | 0.099 |
| 元素的主要化合价 | +1 | +3 | +5、-3 | -2 | +1 | +7、-1 |
| A、X、N元素的金属性:X>N |
| B、Y、M元素形成的离子化合物是工业冶炼Y的原料 |
| C、X单质在M单质中燃烧生成的化合物39g中共含有0.5NA个阴离子 |
| D、标准状况下1L 1mol?L-1的YP3溶液中含有NA个Y3+离子 |
