题目内容
下列说法正确的是( )
| A、凡是没有单质参加的化合反应一定是非氧化还原反应 |
| B、有单质参加的反应一定是氧化还原反应 |
| C、凡是有盐参加的反应都是复分解反应 |
| D、置换反应一定是氧化还原反应 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.有元素的化合价变化为氧化还原反应;
B.氧气转化为臭氧,没有元素的化合价变化;
C.碳酸钠与水、二氧化碳发生化合反应;
D.置换反应置换一定有元素的化合价变化.
B.氧气转化为臭氧,没有元素的化合价变化;
C.碳酸钠与水、二氧化碳发生化合反应;
D.置换反应置换一定有元素的化合价变化.
解答:
解:A.有元素的化合价变化为氧化还原反应,如二氧化硫与过氧化氢反应生成硫酸,为氧化还原反应,没有单质参加,故A错误;
B.氧气转化为臭氧,没有元素的化合价变化,不是氧化还原反应,则有单质参加的反应不一定是氧化还原反应,故B错误;
C.碳酸钠与水、二氧化碳发生化合反应,则有盐参加的反应不一定为复分解反应,故C错误;
D.置换反应置换一定有元素的化合价变化,则一定为氧化还原反应,故D正确;
故选D.
B.氧气转化为臭氧,没有元素的化合价变化,不是氧化还原反应,则有单质参加的反应不一定是氧化还原反应,故B错误;
C.碳酸钠与水、二氧化碳发生化合反应,则有盐参加的反应不一定为复分解反应,故C错误;
D.置换反应置换一定有元素的化合价变化,则一定为氧化还原反应,故D正确;
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意利用实例分析选项,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
相关题目
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是( )
| A、K+、MnO4-、SO42-、Cl- |
| B、Ca2+、HCO3-、NO3-、SO42- |
| C、K+、NO3-、SO42-、CO32- |
| D、Mg2+、SO42-、CO32-、Cl- |
在由NaOH、Na2O2组成的化合物中钠元素的质量分数为58%,则混合物中氢元素的质量分数近似为( )
| A、6% | B、2% |
| C、4% | D、无法确定 |
实验室用密度为1.84g/cm3 98%的浓硫酸与密度为1.1g/cm3 15%的稀硫酸混合配制密度为1.4g/cm3 59%的硫酸溶液,取浓、稀硫酸的体积比最接近的值是( )
| A、1:2 | B、2:1 |
| C、3:2 | D、2:3 |
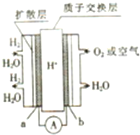 某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )
某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )| A、a极为该电池的负极 |
| B、该电池的正极反应式为O2+4e-+2H2O=4OH- |
| C、多孔活性铂电极有利于吸附气体,增大接触面积 |
| D、H+(质子)由负极移向正极 |
如图,C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则下列说法正确的是( )
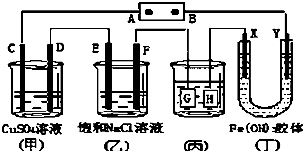

| A、若用乙烷、空气燃料电池作电源,电解质为KOH溶液,则A极的电极反应式为:C2H6-14e-+18OH-=2CO32-+12H2O |
| B、欲用(丙)装置给铜镀银,H应该是Ag,电镀液选是AgNO3溶液 |
| C、(丁)装置中Y极附近红褐色变深,说明氢氧化铁胶体带正电荷 |
| D、C、D、E、F电极均有单质生成,且其物质的量比为1:2:2:2 |
如图是某种微粒的结构示意图,x为( )


| A、8 | B、10 | C、11 | D、无法确定 |
“信息”、“材料”和“能源”被称为新科技革命的三大支柱.下列说法错误的是( )
| A、在即将到来的新能源时代,核能、太阳能、氢能将可能成为主要能源 |
| B、开发太阳能、氢能等新型能源有利于减少二氧化碳的排放量 |
| C、煤的气化技术是减少二氧化碳排放的重要措施 |
| D、煤的“气化”和“液化”技术可提高煤的综合利用效率 |