题目内容
下列叙述正确的是
- A.向NaAlO2溶液中滴加NH4Cl溶液,产生白色沉淀,加入NaHCO3溶液,则不产生沉淀
- B.在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解
- C.将CO2通入Ba(NO3)2溶液中至饱和,无沉淀产生,再通入SO2,产生沉淀
- D.除去FeCl2中少量的FeBr2,加入适量氯水,再加四氯化碳萃取分液
C
分析:A、依据氯化铵水解显酸性,碳酸氢钠除杂电离平衡,偏铝酸酸性弱于碳酸;
B、酸性溶液中硝酸根离子形成稀硝酸具有强氧化性分析判断;
C、酸性溶液中硝酸根离子形成稀硝酸具有强氧化性能氧化二氧化硫为硫酸;
D、亚铁离子还原性大于溴离子,氯气先氧化亚铁离子,在氧化溴离子.
解答:A、向NaAlO2溶液中滴加NH4Cl溶液,产生白色沉淀是因为氯化铵水解显酸性,和偏铝酸根离子结合生成氢氧化铝沉淀,加入NaHCO3溶液,碳酸氢根离子电离出的氢离子和偏铝酸根离子生成氢氧化铝沉淀,促进碳酸氢根离子电离进行,故A错误;
B、在稀硫酸中加入铜粉,根据金属活动顺序可知,铜粉不溶解,再加入Cu(NO3)2固体,溶解后的硝酸根离子和氢离子形成稀硝酸具有强氧化性,铜粉溶解,故B错误;
C、将CO2通入Ba(NO3)2溶液中至饱和,二氧化碳和水反应生成碳酸不与硝酸钡反应,无沉淀产生,再通入SO2,溶液中的稀硝酸能氧化二氧化硫为硫酸,和硝酸钡反应生成硫酸钡产生沉淀,故C正确;
D、除去FeCl2中少量的FeBr2,Fe2+的还原性大于Br-,加入适量氯水,先氧化亚铁离子,再加四氯化碳萃取分液,不能除杂,故D错误;
故选C.
点评:本题考查了盐类水解的应用、电离平衡的移动判断、酸性强弱的反应应用、氧化还原反应的顺序反应判断,关键是分析硝酸根离子在酸性溶液中隐含硝酸具有强氧化性.
分析:A、依据氯化铵水解显酸性,碳酸氢钠除杂电离平衡,偏铝酸酸性弱于碳酸;
B、酸性溶液中硝酸根离子形成稀硝酸具有强氧化性分析判断;
C、酸性溶液中硝酸根离子形成稀硝酸具有强氧化性能氧化二氧化硫为硫酸;
D、亚铁离子还原性大于溴离子,氯气先氧化亚铁离子,在氧化溴离子.
解答:A、向NaAlO2溶液中滴加NH4Cl溶液,产生白色沉淀是因为氯化铵水解显酸性,和偏铝酸根离子结合生成氢氧化铝沉淀,加入NaHCO3溶液,碳酸氢根离子电离出的氢离子和偏铝酸根离子生成氢氧化铝沉淀,促进碳酸氢根离子电离进行,故A错误;
B、在稀硫酸中加入铜粉,根据金属活动顺序可知,铜粉不溶解,再加入Cu(NO3)2固体,溶解后的硝酸根离子和氢离子形成稀硝酸具有强氧化性,铜粉溶解,故B错误;
C、将CO2通入Ba(NO3)2溶液中至饱和,二氧化碳和水反应生成碳酸不与硝酸钡反应,无沉淀产生,再通入SO2,溶液中的稀硝酸能氧化二氧化硫为硫酸,和硝酸钡反应生成硫酸钡产生沉淀,故C正确;
D、除去FeCl2中少量的FeBr2,Fe2+的还原性大于Br-,加入适量氯水,先氧化亚铁离子,再加四氯化碳萃取分液,不能除杂,故D错误;
故选C.
点评:本题考查了盐类水解的应用、电离平衡的移动判断、酸性强弱的反应应用、氧化还原反应的顺序反应判断,关键是分析硝酸根离子在酸性溶液中隐含硝酸具有强氧化性.

练习册系列答案
相关题目
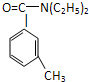 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH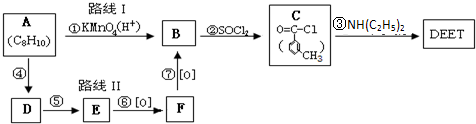
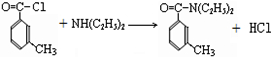
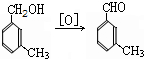
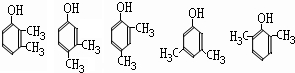 (任写2种)
(任写2种)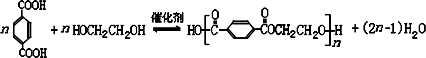
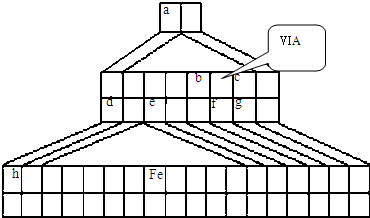
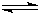 NH3?H2O+H+
NH3?H2O+H+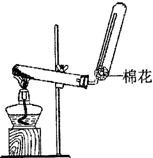 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.