题目内容
一定条件下反应:A2(s)+2B2(g) 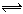 2AB2(g) 达到平衡状态的标志是 ( )
2AB2(g) 达到平衡状态的标志是 ( )
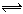 2AB2(g) 达到平衡状态的标志是 ( )
2AB2(g) 达到平衡状态的标志是 ( )| A.V正(B2)==V逆(AB2) |
| B.容器内的总压强不随时间而变化 |
| C.单位时间内生成1molAB2的同时,消耗1mol的B2 |
| D.气体密度不再随时间变化而变化 |
A D
A. 对达到平衡是时,不同物质的正、逆反应速率之比等于化学计量数之比
B 错反应前后气体体积不变,压强不改变,不能用压强判断是否达到平衡
C 错,生成1molAB2,消耗1mol的B2反应方向都是向右的,速率是同一方向,不能判断是否达到平衡
D 对 密度=m/v,气体质量是变化的,体积不变,到平衡时质量不变了,所以密度就不变了,能做为判断平衡的标志。
B 错反应前后气体体积不变,压强不改变,不能用压强判断是否达到平衡
C 错,生成1molAB2,消耗1mol的B2反应方向都是向右的,速率是同一方向,不能判断是否达到平衡
D 对 密度=m/v,气体质量是变化的,体积不变,到平衡时质量不变了,所以密度就不变了,能做为判断平衡的标志。

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示: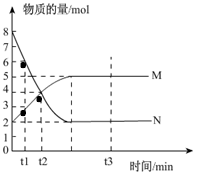
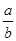 ="_________"
="_________" 
 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)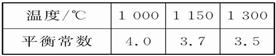
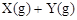
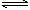
 ;
;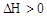 ,下列叙述正确的是( )
,下列叙述正确的是( ) 增大
增大 C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1
C(s)+H2O(g) CO(g)+H2(g) △H=+131.5kJ·mol-1 ③又知C(s)+CO2(g) 2CO(g) △H=+172.5kJ·mol-1
③又知C(s)+CO2(g) 2CO(g) △H=+172.5kJ·mol-1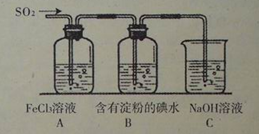


 ,△H
,△H 。在密闭容器中进行,当达到平衡时,欲通过改变条件,达到新平衡后使气体颜色加深,应采取的措施是
。在密闭容器中进行,当达到平衡时,欲通过改变条件,达到新平衡后使气体颜色加深,应采取的措施是
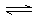 xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示:
xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示: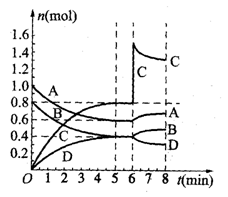
 CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )
CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )