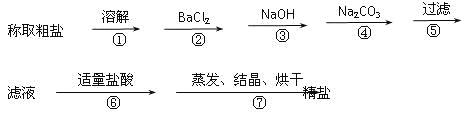
��Ŀ����
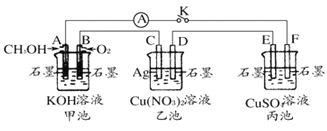
����Ŀ����ij��ȤС���ͬѧ����ͼ��ʾװ���о��йص绯ѧ������![]() �ס��ҡ�����������������
�ס��ҡ�����������������![]() ,���պϸ�װ�õĿ���Kʱ,�۲쵽�����Ƶ�ָ�뷢����ƫת����ش��������⣺
,���պϸ�װ�õĿ���Kʱ,�۲쵽�����Ƶ�ָ�뷢����ƫת����ش��������⣺
(1)�ס��ҡ���������Ϊԭ��ص���______ (�����׳��������ҳ�������������)��
(2)д���׳���A�缫�ĵ缫��Ӧʽ____________��
(3)������F�缫Ϊ______ (����������������������������������������),�óص��ܷ�Ӧ��ѧ����ʽΪ_________��
(4)���ҳ���C�缫��������![]() ʱ,�׳���B�缫����������
ʱ,�׳���B�缫����������![]() �����Ϊ____mL(���)��
�����Ϊ____mL(���)��
(5)һ��ʱ���,�Ͽ�����K������������ʹ���ػָ�����ӦǰŨ�ȵ���____ (��ѡ����ĸ)��
A.Cu ![]()
![]()
![]()
������ʺϵ�����,����Ӧ![]() ,��Ƴ�����ͼ��ʾװ�á���ش��������⣺
,��Ƴ�����ͼ��ʾװ�á���ش��������⣺
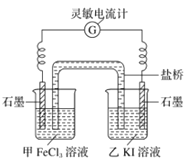
(6)��Ӧ��ʼʱ,����ʯī�缫�Ϸ���___(����������������ԭ��)��Ӧ,�缫��ӦʽΪ_______�������е�__ (����������������)���������Һ�����ƶ���
(7)�����ƶ���Ϊ0ʱ,��Ӧ�ﵽƽ��״̬,��ʱ�ڼ��м���![]() ����,����е�ʯī��______
����,����е�ʯī��______![]() ����������������
����������������![]() ��,�õ缫�ĵ缫��ӦʽΪ_______________��
��,�õ缫�ĵ缫��ӦʽΪ_______________��
(��)���������һ�����Ϳɳ����,����ͨ���ܵ�����,�õ�س�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��![]()
![]()
![]() ��
��
(8)�ŵ�ʱ������ӦΪ______, ���ʱ������ӦΪ_______,�ŵ�ʱ����������Һ�ļ���___![]() ѡ������ǿ��������������������
ѡ������ǿ��������������������![]() ��
��
���𰸡��׳� CH3OH-6e-+8OH-=CO32-+6H2O ���� 2CuSO4+2H2O![]() 2H2SO4+2Cu+O2�� 560 BC ���� 2I--2e-=I2 �� �� Fe2+-e-=Fe3+ Zn-2e-+2OH-�TZn(OH)2 Fe(OH)3-3e-+5OH-=FeO42-+4H2O ��ǿ
2H2SO4+2Cu+O2�� 560 BC ���� 2I--2e-=I2 �� �� Fe2+-e-=Fe3+ Zn-2e-+2OH-�TZn(OH)2 Fe(OH)3-3e-+5OH-=FeO42-+4H2O ��ǿ
��������
��. ��ͼ��֪��ͼΪԭ�����һ�״�ȼ�ϵ�أ�ͨ�״���AΪ������BΪ�������������ҺΪKOH��Һ����A�缫��Ӧ����ʽΪ��2CH3OH+16OH--12e-�TCO32-+12H2O��B�缫��ӦʽΪ��3O2+12e-+6H2O=12OH-���ҳ�Ϊ���أ�CΪ�����缫��ӦΪ��Ag-e-=Ag+��D���������缫��ӦΪCu2++2e-=Cu������Ϊ���أ�EΪ�������缫��ӦΪ��4OH--4e-=O2��+2H2O��F�缫Ϊ�������缫��ӦΪ��Cu2++2e-=Cu�����ܷ�Ӧ����ʽΪ��2CuSO4+2H2O![]() 2H2SO4+2Cu+O2����һ��ʱ��Ͽ����K��Ҫʹ���ػָ�����ӦǰŨ�������CuO����CuCO3���ݴ˷������
2H2SO4+2Cu+O2����һ��ʱ��Ͽ����K��Ҫʹ���ػָ�����ӦǰŨ�������CuO����CuCO3���ݴ˷������
��. (6) ��Ӧ��ʼʱ�����е�����ʧ���ӷ���������Ӧ���缫��ӦʽΪ��2I--2e-=I2��Fe3+����ԭ��Fe2+��������ԭ��Ӧ���缫��ӦʽΪ��Fe3++e-=Fe2+�������е����������������ƶ���
(7) ��Ӧ�ﵽƽ�������м�������FeCl2���壬Fe2+Ũ������ƽ�������ƶ�����Fe2+ʧȥ��������Fe3+��
��. (8) �ŵ�ʱ��Zn����������Zn(OH)2��������Ϊ���أ�Fe(OH)3ʧȥ��������K2FeO4���ŵ�ʱ���������������������ӡ�
��.(1) ��ͼ��֪�׳�Ϊԭ��أ�
(2) ��ͼ��֪��ͼΪԭ�����һ�״�ȼ�ϵ�أ�ͨ�״���AΪ�������缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��
(3)������F�缫��ȼ�ϵ�صĸ�����������F�缫Ϊ���ص��������óص��ܷ�Ӧ��ѧ����ʽΪ2CuSO4+2H2O![]() 2H2SO4+2Cu+O2����
2H2SO4+2Cu+O2����
(4) �ҳ�Ϊ���أ�CΪ�����缫��ӦΪ��Ag-e-=Ag+��D���������缫��ӦΪCu2++2e-=Cu���ҳ���C����������10.8g���������ʵ���n(Ag)=![]() =0.1mol����ת�Ƶ���Ϊ0.1mol���ʼ׳�����O2Ϊ0.1 mol��
=0.1mol����ת�Ƶ���Ϊ0.1mol���ʼ׳�����O2Ϊ0.1 mol��![]() =0.025mol���������Ϊ0.025 mol��22.4L/mol=0.56L=560mL��
=0.025mol���������Ϊ0.025 mol��22.4L/mol=0.56L=560mL��
(5) һ��ʱ��Ͽ����K��Ҫʹ���ػָ�����ӦǰŨ�ȣ�����2CuSO4+2H2O![]() 2H2SO4+2Cu+O2����֪�������CuO����CuCO3��CuO��������������ͭ��ˮ��CuCO3��������������ͭ��������̼��ˮ���ʴ�ΪBC��
2H2SO4+2Cu+O2����֪�������CuO����CuCO3��CuO��������������ͭ��ˮ��CuCO3��������������ͭ��������̼��ˮ���ʴ�ΪBC��
��.(6) ��Ӧ��ʼʱ�����е�����ʧ���ӷ���������Ӧ��Ϊ���������缫��ӦʽΪ��2I--2e-=I2�������е����������������ƶ����������Һ�����ƶ���
(7) ��Ӧ�ﵽƽ�������м�������FeCl2���壬Fe2+Ũ������ƽ�������ƶ�����Fe2+ʧȥ��������Fe3+���׳��е�ʯī�������������ĵ缫��ӦʽΪFe2+-e-=Fe3+��
��. (8) �ŵ�ʱ��Zn����������Zn(OH)2���Ǹ���������ӦʽΪ��Zn-2e-+2OH-�TZn(OH)2��������Ϊ���أ����ʱ������Fe(OH)3ʧȥ��������K2FeO4���缫��ӦʽΪ��Fe(OH)/span>3-3e-+5OH-=FeO42-+4H2O���ŵ�ʱ���������������������ӣ���Һ�ļ�����ǿ��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ����Ԫ����һ����Ҫ�ķǽ���Ԫ�أ����γɶ��ֻ�����Իش������й����⣺
��1������֪4CO(g)+2NO2(g)4CO2(g)+N2(g) ��H=-1200kJmol-1�����ڸ÷�Ӧ���ı�ijһ��Ӧ������(��֪�¶�T2>T1)����ͼ����ͼ1��ȷ����___(�����)��

����֪CO��H2O��һ�������¿��Է�����Ӧ��CO(g)+H2O(g)CO2(g)+H2(g) ��H=-QkJmol-1��820��ʱ���ڼס������������ܱ������У���ʼʱ�����±�����Ͷ�ϣ�����һ��ʱ���ﵽƽ��״̬��������CO��ת����Ϊ40%����÷�Ӧ��ƽ�ⳣ��Ϊ___�����������յ�����Ϊ___��
�� | �� |
0.10molH2O | 0.20molH2 |
0.10molCO | 0.20molCO2 |
��2����ˮ����������������֪25��ʱ��Ksp[Fe(OH)3]=2.6��10-39��Ksp[Al(OH)3]=1.1��10-33����Ũ�Ⱦ�Ϊ0.1molL-1��FeCl3��AlCl3�����Һ�м��백ˮ���������ɵij�����___(�ѧʽ)��
��3���¿���Ϊ�����������ȼ�ϣ���������N2O4��Ӧ����N2��ˮ��������֪��
��N2(g)+2O2(g)=N2O4(l) ��H=-19.5kJmol-1
��N2H4(l)+O2(g)=N2(g)+2H2O(g) ��H=-534.2kJmol-1
д������������������Ӧ���Ȼ�ѧ����ʽ___��
��4�����ĵ�����(HN3)����ɫҺ�壬����������������������25mL0.1molL-1NaOH��Һ�м���0.2molL-1HN3����Һ���μӹ����е�pHֵ�ı仯����(��Һ���ʱ������仯���Բ���)��ͼ2��

�ٸ���ͼ��д��HN3�ĵ��뷽��ʽ��___��
������˵����ȷ����___(�����)��
A.������֪Ũ�ȵ�NaOH��Һ�ζ�HN3��Һ���ⶨHN3��Ũ��ʱӦ�ü�����ָʾ��
B.�����£���0.2molL-1HN3����Һ�м�ˮϡ�ͣ���![]() ����
����
C.�ֱ��к�pH��Ϊ4��HN3��Һ��HCl��Һ������0.1molL-1NaOH��Һ�������ͬ
D.D��ʱ��Һ������Ũ�ȴ������¹�ϵ��2c(H+)+c(HN3)=c(N3-)+2c(OH-)
����Ŀ���������������ʵ�Ľ�����ȷ����![]()
ѡ�� | �������ʵ | ���� |
A | ���ȵĴ�����Һϴȥ���� |
|
B | Ư���ڿ����о��ñ��� | Ư���е� |
C | ʩ��ʱ����ľ�� |
|
D | �����ڳ�ʪ�Ŀ������������� | �����ڿ����з��������ⸯʴ |
A.AB.BC.CD.D