题目内容
某温度下,将Cl2通入氢氧化钾溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO
离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
- 3 |
| A、2:3 | B、4:3 |
| C、10:3 | D、11:3 |
考点:氧化还原反应的计算
专题:计算题
分析:Cl2生成ClO-、ClO3-化合价升高,是被氧化的过程,而Cl2生成NaCl是化合价降低被还原的过程,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,根据ClO-与ClO3-的物质的量浓度之比可计算出失去电子的总物质的量,进而可计算得到电子的总物质的量;再根据氯元素被还原生成KCl的化合价变化为1计算出被还原的氯元素的物质的量,最后计算出被还原的氯元素和被氧化的氯元素的物质的量之比.
解答:
解:Cl2生成ClO-与ClO3-是被氧化的过程,化合价分别由0价升高为+1价和+5价,
经测定ClO-和ClO3-物质的量之比为1:2,
则可设ClO-为1mol,ClO3-为2mol,被氧化的氯元素的物质的量为:1mol+2mol=3mol,
根据化合价变化可知,反应中失去电子的总物质的量为:1mol×(1-0)+2mol×(5-0)=11mol,
氧化还原反应中得失电子数目一定相等,则该反应中失去电子的物质的量也是11mol,
Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,
则被还原的Cl的物质的量为:
=11mol,
所以被还原的氯元素和被氧化的氯元素的物质的量之比为11mol:3mol=11:3,
故选D.
经测定ClO-和ClO3-物质的量之比为1:2,
则可设ClO-为1mol,ClO3-为2mol,被氧化的氯元素的物质的量为:1mol+2mol=3mol,
根据化合价变化可知,反应中失去电子的总物质的量为:1mol×(1-0)+2mol×(5-0)=11mol,
氧化还原反应中得失电子数目一定相等,则该反应中失去电子的物质的量也是11mol,
Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,
则被还原的Cl的物质的量为:
| 11mol |
| 1-0 |
所以被还原的氯元素和被氧化的氯元素的物质的量之比为11mol:3mol=11:3,
故选D.
点评:本题考查氧化还原反应的计算,题目难度中等,注意掌握氧化还原反应的实质、特征,能够根据化合价变化判断得失电子总数,明确电子守恒在化学计算中的应用方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、硫酸铝溶液和小苏打溶液反应:Al3++3HCO3-═3CO2↑+Al(OH)3↓ |
| B、向Ca(ClO)2溶液中通入二氧化硫:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| C、硫化亚铁中加入盐酸:S2-+2H+═H2S↑ |
| D、钠和冷水反应:Na+2H2O═Na++H2↑+2OH- |
下列各组物质中,一定互为同系物的是( )
| A、核糖和脱氧核糖 |
| B、分子式为C4H6和C5H8的烃 |
| C、葡萄糖和蔗糖 |
| D、分子式为C4H10和C20H42的烃 |
下列有关物质的性质、制取或应用等的说法中正确的是( )
| A、用10%的盐酸蒸发浓缩获得30%的盐酸 |
| B、可利用丁达尔效应来区别淀粉溶液和氯化钠溶液 |
| C、二氧化硫具有漂白性,与氯水混合使用效果更好 |
| D、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
下列关于胶体的认识错误的是( )
| A、布朗运动是胶体能稳定存在的次要原因 |
| B、纳米材料粒子直径一般从几纳米到几十纳米(1 nm=10-9 m),因此纳米材料属于胶体 |
| C、往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 |
| D、电泳可以用于某些物质的分离和提纯 |
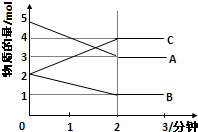 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.则该反应的反应物是
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.则该反应的反应物是 在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O42NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O42NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)