题目内容
某有机物中只含C、H、O三种元素,相对分子质量为46,2.3g该物质完全燃烧后生成0.1mol二氧化碳和2.7g水,该化合物的分子式为 根据C、H、O三种元素在有机物中的价键特征,请你推测乙醇具有的可能的结构简式: .
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据n=
计算出水的物质的量,再根据质量守恒计算出2.3g该有机物中含有的C、H元素的物质的量、质量及氧元素的质量、物质的量,再根据n(C):n(H):n(O)计算出该有机物的实验式,结合相对分子量确定其分子式;根据乙醇含有的官能团确定乙醇的结构简式.
| m |
| M |
解答:
解:2.3g该有机物完全燃烧产物为H2O和CO2,2.7g水的物质的量为:n(H2O)=
=0.15mol,则n(H)=0.15mol×2=0.3mol,m(H)=1g/mol×0.3mol=0.3g;
二氧化碳的物质的量为:n(CO2)=0.1mol,则n(C)=0.1mol,m(C)=12g/mol×0.1mol=1.2g,
该有机物中氧元素的质量为:m(O)=2.3g-1.2g-0.3g=0.8g,n(O)=
=0.05mol,
该有机物分子中:n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6:1,
该物质的实验式为C2H6O,设其分子式为 (C2H6O)n,有机物相对分子质量为46,则n=
=1,
则有机物的分子式为:C2H6O;
乙醇分子中含有羟基,乙醇的结构简式为:C2H6OCH3CH2OH,
故答案为:C2H6O;CH3CH2OH.
| 2.7g |
| 18g/mol |
二氧化碳的物质的量为:n(CO2)=0.1mol,则n(C)=0.1mol,m(C)=12g/mol×0.1mol=1.2g,
该有机物中氧元素的质量为:m(O)=2.3g-1.2g-0.3g=0.8g,n(O)=
| 0.8g |
| 16g/mol |
该有机物分子中:n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6:1,
该物质的实验式为C2H6O,设其分子式为 (C2H6O)n,有机物相对分子质量为46,则n=
| 46 |
| 46 |
则有机物的分子式为:C2H6O;
乙醇分子中含有羟基,乙醇的结构简式为:C2H6OCH3CH2OH,
故答案为:C2H6O;CH3CH2OH.
点评:本题考查了有机物分子式、结构简式的确定,题目难度中等,注意掌握常见有机物的分子式的计算方法,能够正确书写常见有机物的结构简式,注意质量守恒定律在计算中的应用.

练习册系列答案
相关题目
某温度下,将Cl2通入氢氧化钾溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO
离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
- 3 |
| A、2:3 | B、4:3 |
| C、10:3 | D、11:3 |
在恒温恒容的容器中进行反应N2O4(g)?2NO2(g)△H>0,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么,反应物浓度由0.06mol/L降到0.024mol/L,需反应的时间为( )
| A、等于18 s |
| B、等于12 s |
| C、大于18s |
| D、小于18s |
把生铁冶炼成碳素钢要解决的主要问题是( )
| A、除去生铁中的各种杂质,把生铁提纯 |
| B、适当降低生铁里的含碳量,除去大部分硫、磷等有害杂质 |
| C、用还原剂把铁的氧化物还原成铁 |
| D、加入合金元素改善生铁性能 |
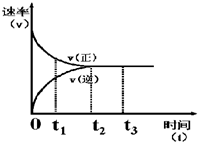 如图是可逆反应X+Y?Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )
如图是可逆反应X+Y?Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不正确的是( )| A、t1时,正反应速率大于逆反应速率 |
| B、t2时,达到该条件下的最大反应限度 |
| C、t2-t3,反应不再发生,各物质的浓度相等 |
| D、t3后,该反应的反应限度有可能被外界条件改变 |
