题目内容
向100mL 1mol/L硫酸铝铵![]() 溶液中,逐滴加入1mol/L的
溶液中,逐滴加入1mol/L的![]() 溶液.
溶液.
(1)当生成沉淀的物质的量的总量最大时的离子方程式是(用一个离式方程式表示)__________________________________.
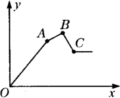
(2)随着![]() 溶液的加入,沉淀总的物质的量(Y轴)与
溶液的加入,沉淀总的物质的量(Y轴)与![]() 溶液的体积(X轴)的关系如图所示,则A、C两点对应的
溶液的体积(X轴)的关系如图所示,则A、C两点对应的![]() 溶液的体积为:
溶液的体积为:
A ________mL C ________mL
答案:
解析:
解析:
|
答案:(1) (2)150,250 解析:(1)本题反应较为复杂,当加入 (2)应搞清A、B、C三点的含义.A点为 |

练习册系列答案
相关题目
