题目内容
15.下列比较中,正确的是( )| A. | 同温度同物质的量浓度时,HF比HCN易电离,NaF溶液的pH比NaCN溶液大 | |
| B. | 0.2 mol•L-1NH4Cl和0.1 mol•L-1 NaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 同浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3•H2O;c(NH4+)由大到小的顺序是:①>②>③>④ | |
| D. | 物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
分析 A.相同温度相同浓度时HF比HCN易电离说明HF酸性大于HCN,酸性越强其相应酸根离子水解程度越小,相同浓度的钠盐溶液pH越小;
B.0.2 mol•L-1NH4Cl和0.1 mol•L-1 NaOH溶液等体积混合后,溶液中的溶质为等物质的量浓度的NH4Cl、NH3.H2O、NaCl,一水合氨电离程度大于铵根离子水解程度导致溶液呈碱性,根据物料守恒和电荷守恒判断;
C.相同浓度时铵根离子水解程度越大,则溶液中铵根离子浓度越小,铝离子抑制铵根离子水解、醋酸根离子促进铵根离子水解;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
解答 解:A.相同温度相同浓度时HF比HCN易电离说明HF酸性大于HCN,酸性越强其相应酸根离子水解程度越小,相同浓度的钠盐溶液pH越小,水解能力CN->F-,所以相同浓度的钠盐溶液pHNaF<NaCN,故A错误;
B.0.2 mol•L-1NH4Cl和0.1 mol•L-1 NaOH溶液等体积混合后,溶液中的溶质为等物质的量浓度的NH4Cl、NH3.H2O、NaCl,一水合氨电离程度大于铵根离子水解程度导致溶液呈碱性,则c(OH-)>c(H+),一水合氨电离但程度较小,结合物料守恒得c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),故B错误;
C.相同浓度时铵根离子水解程度越大,则溶液中铵根离子浓度越小,铝离子抑制铵根离子水解、醋酸根离子促进铵根离子水解,一水合氨是弱电解质,电离程度较小,所以c(NH4+)由大到小的顺是:①>②>③>④,故C正确;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-),故D错误;
故选C.
点评 本题考查离子浓度大小比较,为高频考点,明确溶液中溶质及其性质是解本题关键,结合电荷守恒、物料守恒判断,注意B中溶液成分及其浓度关系,题目难度不大.

①将小块钠投入滴有石蕊试液的水中,反应后溶液变红
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④钠与氧气反应的产物为过氧化钠.
| A. | 只有①② | B. | 只有②③ | C. | 只有②③④ | D. | ①②③④ |
( )

| A. | CO、SO2、SO3均是酸性氧化物 | |
| B. | 工业上利用Cl2和澄清石灰水反应来制取漂白粉 | |
| C. | 漂白粉的有效成分为Ca(ClO)2 | |
| D. | 除去与水反应的两个反应,图示其余转化反应均为氧化还原反应 |
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体一定含CO32- | |
| B. | 某无色溶液滴入酚酞试液显红色,该溶液呈碱性 | |
| C. | 某溶液中滴加BaCl2溶液生成不溶于稀硝酸的白色沉淀,该溶液可能含有SO42- | |
| D. | 验证烧碱溶液中是否含Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl- |
| A. | 过氧化钠加到冷水中:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 过量氢氧化钠溶液与氯化铝溶液反应:Al3++3OH-═Al(OH)3↓ | |
| C. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO${\;}_{2}^{-}$+H2O | |
| D. | 氢氧化钡溶液中加入稀硫酸:H++OH-═H2O |
| A. | 一个D2O分子所含的中子数为8 | B. | NH3的结构式为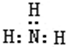 | ||
| C. | HCl的电子式为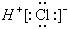 | D. | 热稳定性:H2S<HF |
| 选项 | 试剂 | 湿润的试纸 | 现象 | 结论 |
| A | Na2SO3,浓硫酸 | 品红试纸 | 褪色 | SO2具有漂白性 |
| B | 浓氨水,生石灰 | 蓝色石蕊试纸 | 变红 | 氨气为碱性气体 |
| C | 碘水 | 淀粉试纸 | 变蓝 | 碘具有氧化性 |
| D | Cu,浓硝酸 | 淀粉-KI试纸 | 变蓝 | NO2为酸性气体 |
| A. | A | B. | B | C. | C | D. | D |
| 二氧化碳 | 碳酸钠 | 转移的电子 | |
| A | 1mol | NA | |
| B | 22.4L | 1mol | |
| C | 212g | 1mol | |
| D | 106g | 2NA |
| A. | A | B. | B | C. | C | D. | D |