题目内容
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素,由Y元素组成的单质通常呈淡黄色.
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式是 .
(2)Y 的低价氧化物通入Z单质的水溶液中,发生的化学反应方程式是 .
(3)比较Y、Z气态氢化物的稳定性 (用化学式表示).
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是 (用离子符号表示).
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式是
(2)Y 的低价氧化物通入Z单质的水溶液中,发生的化学反应方程式是
(3)比较Y、Z气态氢化物的稳定性
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:W、X、Y、Z是原子序数依次增大的同一短周期元素,由Y元素组成的单质通常呈淡黄色,则Y为S,即元素均在第三周期,Z应为Cl,
(1)W、X是金属元素,W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,则W为Na,X为Al;
(2)Y 的低价氧化物通入Z单质的水溶液中,应为二氧化硫与氯水的反应;
(3)非金属性越强,气态氢化物越稳定;
(4)离子的电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半径小.
(1)W、X是金属元素,W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,则W为Na,X为Al;
(2)Y 的低价氧化物通入Z单质的水溶液中,应为二氧化硫与氯水的反应;
(3)非金属性越强,气态氢化物越稳定;
(4)离子的电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半径小.
解答:
解:W、X、Y、Z是原子序数依次增大的同一短周期元素,由Y元素组成的单质通常呈淡黄色,则Y为S,即元素均在第三周期,Z应为Cl,
(1)W、X是金属元素,W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,则W为Na,X为Al,它们的最高价氧化物的水化物反应的离子反应为Al(OH)3+OH-═AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)Y、Z是非金属元素,Y的低价氧化物通入Z单质的水溶液中,则Z为Cl,二氧化硫和氯气反应生成盐酸与硫酸,该反应为SO2+C12+2H2O═H2SO4+2HCl,
故答案为:SO2+Cl2+2H2O=H2SO4+2HCl;
(3)非金属性Cl>S,气态氢化物的稳定性HCl>H2S,故答案为:HCl>H2S;
(4)离子的电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半径小,则离子半径大小为S2->Cl->Na+>Al3+,
故答案为:r(S2-)>r(Cl-)>r(Na+)>r(Al3+).
(1)W、X是金属元素,W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,则W为Na,X为Al,它们的最高价氧化物的水化物反应的离子反应为Al(OH)3+OH-═AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)Y、Z是非金属元素,Y的低价氧化物通入Z单质的水溶液中,则Z为Cl,二氧化硫和氯气反应生成盐酸与硫酸,该反应为SO2+C12+2H2O═H2SO4+2HCl,
故答案为:SO2+Cl2+2H2O=H2SO4+2HCl;
(3)非金属性Cl>S,气态氢化物的稳定性HCl>H2S,故答案为:HCl>H2S;
(4)离子的电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半径小,则离子半径大小为S2->Cl->Na+>Al3+,
故答案为:r(S2-)>r(Cl-)>r(Na+)>r(Al3+).
点评:本题考查位置、结构、性质的关系,熟悉第三周期元素的性质变化规律及常见元素的单质和化合物的性质是解答本题的关键,难度不大.

练习册系列答案
相关题目
下列有关元素化合物的说法中正确的是( )
| A、在金属活性顺序表中,Na排在Cu的前面,所以Na可与CuSO4溶液反应置换出单质Cu |
| B、用金属铝可做导线或炊具,是因为金属铝能导热且铝在空气中很稳定 |
| C、金属钠之所以保存在煤油中,是因为煤油能隔绝空气、水分,而且Na的密度比煤油大 |
| D、金属铝在生产生活中应用很广,但价格便宜,这是因为铝元素在地壳中含量第一 |
下列说法正确的是( )
| A、所有苯的同系物中滴加3-5滴酸性高锰酸钾溶液,振荡并稍稍加热,均可观察到溶液褪色 |
| B、甘氨酸和丙氨酸脱水,最多可生成3种二肽 |
| C、在高浓度的铜氨溶液中加入脱脂棉,搅拌成黏稠液,用注射器将吸入的黏稠液注入稀盐酸中,将生成物水洗后可获得铜氨纤维 |
| D、欲检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2并加热 |
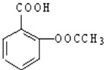 ,难溶于水.为了使疗效更好,它可与
,难溶于水.为了使疗效更好,它可与