题目内容
18.(1)下列物质:①NaCl晶体 ②SO3 ③冰醋酸 ④铜 ⑤BaSO4固体⑥纯蔗糖⑦酒精 ⑧熔融的KNO3 ⑨空气,⑩食盐水,请回答下列问题(用序号填空):(Ⅰ)能导电的是④⑧⑩;
(Ⅱ)属于电解质的是①③⑤⑧;
(Ⅲ)属于非电解质的是②⑥⑦;
(Ⅳ)溶于水后形成的溶液能导电的是①②③⑧.
(2)18gNH4+中含有氢原子的物质的量是4mol;含有质子的物质的量是11mol;含有电子的数目是10NA.
分析 (1)(Ⅰ)物质能够导电,说明该物质中存在自由移动的电子或离子;
(Ⅱ)在水溶液中或熔化状态下能导电的化合物为电解质;
(Ⅲ)在水溶液中和熔化状态下都不能导电的化合物为非电解质;
(Ⅳ)在水溶液中能够导电,说明在溶液中能够电离出自由移动的离子;
(2)根据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$结合分子、原子的构成计算.
解答 解:(1)(Ⅰ)以上物质存在自由移动的电子或离子,能导电的有④铜 ⑧熔融的KNO3 ⑩食盐水,
故答案为:④⑧⑩;
(Ⅱ)电解质为:在水溶液中或熔化状态下能导电的化合物,满足条件的有:①NaCl晶体 ③冰醋酸 ⑤BaSO4固体⑧熔融的KNO3,
故答案为:①③⑤⑧;
(Ⅲ)非电解质为在水溶液中和熔化状态下都不能导电的化合物,满足条件的有 ②SO3 ⑥纯蔗糖⑦酒精,
故答案为:②⑥⑦;
(Ⅳ)溶液中能够导电的有:①NaCl晶体 ②SO3 ③冰醋酸 ⑧熔融的KNO3,
故答案为:①②③⑧;
(2)n(NH4+)=$\frac{18}{18}$=1mol,所以氢原子的物质的量是4mol;含有质子的物质的量是11×1=11mol;含有电子的数目是10×1×NA=10NA,
故答案为:4mol;11mol;10NA.
点评 本题考查了电解质、非电解质的判断、溶液的导电性判断以及物质的量的相关计算,题目难度不大,注意掌握电解质和非电解质的概念及判断方法,能够明确物质导电性与电解质的关系,试题有利于提高学生灵活应用所学知识的能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
8.关于铁生锈的说法正确的是( )
| A. | 铁锈的主要成分是Fe(OH)3 | |
| B. | 铁锈蚀过程中只发生了氧化还原反应 | |
| C. | 铁锈蚀与环境湿度和铁件密封程度有关 | |
| D. | 铁件发生电化学腐蚀时的负极反应式为Fe-3e-═Fe3+ |
6.下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
| A. | 硫酸、CuSO4•5H2O、苛性钾 | B. | 硫酸、空气、纯碱 | ||
| C. | 硝酸、食盐水、烧碱 | D. | 氧化铁、胆矾、熟石灰 |
13.下列物质属于钠盐的是( )
| A. | NaHSO4 | B. | NaOH | C. | Na2O | D. | Na2O2 |
3.下列有机物的命名正确的是( )
| A. |  2-乙基丙烷 2-乙基丙烷 | B. | CH3CH2CH2CH2OH 1-丁醇 | ||
| C. |  间二甲苯 间二甲苯 | D. |  2-甲基-2-丙烯 2-甲基-2-丙烯 |
7.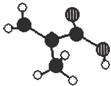 北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
 北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )| A. | 该产品的名称是甲基丙酸 | |
| B. | 该产品与硬脂酸互为同系物 | |
| C. | 四个黑球一定在同一个平面上 | |
| D. | 一定条件下,可以与乙二醇发生酯化反应,也可与氯化氢发生加成反应且产物只有一种 |
8.对于如图所示装置的叙述正确的是( )
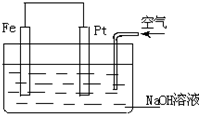

| A. | 这是一个原电池的装置 | |
| B. | 这是电解NaOH溶液的装置 | |
| C. | Pt为正极,其电极反应为:2H++2e-═H2↑ | |
| D. | Fe为负极,其电极反应为:4OH--4e-═2H2O+O2↑ |
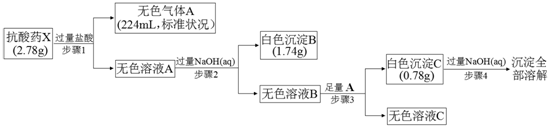
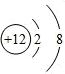 ,A的电子式为
,A的电子式为 .
.