��Ŀ����
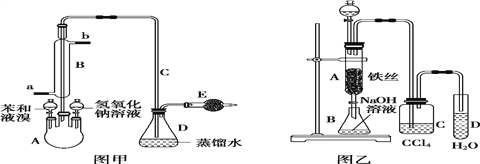
����Ŀ���йش����Ĵ�������������Դӡ��Ҵ�������ʵ�顱�õ�һЩ��ʶ,ij��ʦ�������ͼ��ʾװ��(�г�װ�õ���ʡ��),��ʵ�����Ϊ:�Ȱ�ͼ��װ��װ��,�رջ���a��b��c,��ͭ˿���м䲿�ּ���Ƭ��,Ȼ�����a��b��c,ͨ�����ƻ���a��b,���н���(��Ъ��)��ͨ������,������M���۲쵽���Ե�ʵ�������Իش���������:

��1��A�з�����Ӧ�Ļ�ѧ����ʽ:_____________________________________,
B������:_____________________;C����ˮ������:________________________________��
(2)M��������Ӧ�Ļ�ѧ����ʽΪ________________________________��
(3)��M���пɹ۲쵽������:_________________________________��
(4)ʵ�����һ��ʱ���,��������ƾ���,��Ӧ__(��ܡ����ܡ�)��������,��ԭ����______________________________________________________________________��
(5)��֤�Ҵ���������Ļ�ѧ������____________________________��
���𰸡� 2H2O2![]() 2H2O+O2�� ����O2 ʹD���Ҵ���Ϊ��������M�μӷ�Ӧ,��ˮԡ����ʹ�Ҵ�������ƽ�� 2CH3CH2OH+O2
2H2O+O2�� ����O2 ʹD���Ҵ���Ϊ��������M�μӷ�Ӧ,��ˮԡ����ʹ�Ҵ�������ƽ�� 2CH3CH2OH+O2![]() 2CH3CHO+2H2O ���Ȳ��ֵ�ͭ˿������ֱ�ڡ��������� �� �Ҵ��Ĵ�������Ӧ�Ƿ��ȷ�Ӧ,��Ӧ�ų���������ά�ַ�Ӧ�������� ʵ�������,ж��װ��F��ʢ����������ˮ���Թ�,����ȡ��������Һ��������Ӧʵ��[Ҳ��ʹ֮������Cu(OH)2����Һ��Ӧ],��֤����ȩ������
2CH3CHO+2H2O ���Ȳ��ֵ�ͭ˿������ֱ�ڡ��������� �� �Ҵ��Ĵ�������Ӧ�Ƿ��ȷ�Ӧ,��Ӧ�ų���������ά�ַ�Ӧ�������� ʵ�������,ж��װ��F��ʢ����������ˮ���Թ�,����ȡ��������Һ��������Ӧʵ��[Ҳ��ʹ֮������Cu(OH)2����Һ��Ӧ],��֤����ȩ������
��������(1)A���ǹ��������ڶ������̴�����������ˮ����������Ӧ�Ļ�ѧ����ʽΪ2H2O2 ![]() 2H2O+O2����B�����������е�ˮ������C��ˮԡ�����Ҵ��õ�������ƽ�ȵ��Ҵ���������M���ʴ�Ϊ��2H2O2
2H2O+O2����B�����������е�ˮ������C��ˮԡ�����Ҵ��õ�������ƽ�ȵ��Ҵ���������M���ʴ�Ϊ��2H2O2 ![]() 2H2O+O2������������(�����������е�ˮ)�� ʹD���Ҵ���Ϊ��������M�вμӷ�Ӧ����ˮԡ����ʹ�Ҵ�������ƽ�ȣ�
2H2O+O2������������(�����������е�ˮ)�� ʹD���Ҵ���Ϊ��������M�вμӷ�Ӧ����ˮԡ����ʹ�Ҵ�������ƽ�ȣ�
(2)��ͭ�����������������£��Ҵ��ܱ���������������ȩ��ˮ������M��������Ӧ�Ļ�ѧ����ʽΪ2CH3CH2OH+O2![]() 2CH3CHO+2H2O���ʴ�Ϊ��2CH3CH2OH+O2
2CH3CHO+2H2O���ʴ�Ϊ��2CH3CH2OH+O2![]() 2CH3CHO+2H2O��
2CH3CHO+2H2O��
(3)�Ҵ��Ĵ�������Ӧ�У�����ͭ���������������Ҵ���Ӧ���������õ�������ͭ��ʵ�������ͭ�����ֺ�ɫ��������ͭ��������Ӧ��������ͭ����Ӧ�ķ���ʽΪ2Cu+O2![]() 2CuO��ͭ���ɺ�ɫ��ɺ�ɫ�������Ҵ�������ͭ��Ӧ����ͭ����Ӧ�ķ���ʽΪCH3CH2OH+CuO
2CuO��ͭ���ɺ�ɫ��ɺ�ɫ�������Ҵ�������ͭ��Ӧ����ͭ����Ӧ�ķ���ʽΪCH3CH2OH+CuO![]() CH3CHO+Cu+H2O��������Ȳ��ֵ�ͭ˿������ֱ�ڡ��������ʴ�Ϊ�����Ȳ��ֵ�ͭ˿������ֱ�ڡ���������
CH3CHO+Cu+H2O��������Ȳ��ֵ�ͭ˿������ֱ�ڡ��������ʴ�Ϊ�����Ȳ��ֵ�ͭ˿������ֱ�ڡ���������
(4)�����ƾ��ƣ���Ӧ�Խ��У����Ĵ�������Ӧ�Ƿ��ȷ�Ӧ���ų����������㷴Ӧ�����¶ȣ��ʴ�Ϊ���ܣ��Ҵ��Ĵ�������Ӧ�Ƿ��ȷ�Ӧ����Ӧ�ų���������ά�ַ�Ӧ�������У�
(5)�Ҵ�������Ϊ��ȩ����ȩ����ȩ�������л�ԭ�ԣ��ܱ�������Һ������������ͭ����Һ�����������֤�Ҵ���������Ļ�ѧ�����ǣ�ʵ�������ж��װ��F��ʢ����������ˮ���Թ��У��������Ƶ�������Һˮԡ���ȣ��۲��Թܱ����й������������ɣ���ȡ�����������������Թ��У��������Ƶ�������ͭ����Һ���ȣ��۲��к�ɫ�ij������ɣ��ʴ�Ϊ��ʵ�������ж��װ��F��ʢ����������ˮ���Թܣ�����ȡ��������Һ��������Ӧʵ��[Ҳ��ʹ֮������Cu(OH)2����Һ��Ӧ]����֤����ȩ�����ɡ�

����Ŀ��������ʯβ������ȡNiSO4�ǽ���ҹ�����Դ�ѷ���һ����Ҫ;������֪�ù������£�
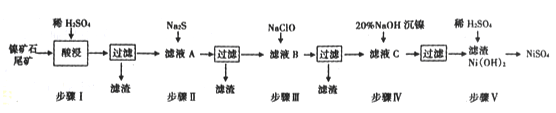
��1�������ʵ�Ksp�������±���
���� | MnS | NiS | PbS | CuS | Ni(OH)2 |
Ksp | 2.5��10-13 | 1.1��10-21 | 8.0��10-28 | 6.3��10-36 | 2.0��10-15 |
��2����ҺA�и��������ӵĺ������±���
�ɷ� | Ni2+ | Fe3+ | Fe2+ | Mn2+ | Cu2+ | Pb2+ | ���� |
3.80 | 4.80 | x | 0. 20 | 0.15 | <0.001 | ���� |
����������Ϣ���ش��������⣺
(1)����I���֮ǰ�轫��ʯ���飬Ŀ����____________��
(2)���������ӵ�Ũ��c��1.0��10-5mol/L�����϶�������ȫ��������е�Pb2+��ǡ�ó�����ȫʱ����Һ�������ӵ�Ũ��c(S2-)=_____________
(3)�����½��в�����Ŀ����Ϊ�˳�ȥ������Ԫ�أ���֪����Ԫ�ص����ӷ�Ӧ���£�
2Fe2++ ClO - +5H2O=2Fe( OH)3��+Cl-+4H+
��ʱMn2+����������ΪMnO2��д������Ԫ�ص����ӷ���ʽ______________��
(4)Ϊ�ⶨ��ҺA��Fe2+���ӵĺ�������ÿ����Һ�к��е��������ӵ���������g/L��ʾ��ÿ����ȡ20.00 mL����Һ������0.02 mol/L��KMnO4��Һ�ζ�������֪�������Ӿ�����Ӧ�������εζ�ƽ������KMnO4��Һ18. 00mL����x��ֵΪ________����ȷ��С�������λ����
��5������Ni(OH)2���������ӵ�ص���Ҫԭ�ϣ����ӵ�ع���ԭ�����£�
Cd+2NiO(OH) +2H2O![]() Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
�����ŷŵ�Ľ��У�������pH______�����������С�����䡱�������ʱ�����缫��ӦʽΪ______��