题目内容
解释下列原因。(1)埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀
(2)为保护海轮的船壳,常在船壳上镶入锌块
(3)在空气中,金属银的表面生成一层黑色物质
(4)镀银的铁制品,镀层部分受损后,露出的铁表面易被腐蚀
解析:(1)潮湿土壤中的铁管易形成原电池发生电化腐蚀;干燥土壤的铁管通常发生化学腐蚀。
(2)形成Zn-Fe原电池,Zn比Fe活泼,被腐蚀,释放出电子保护Fe:Zn![]() Zn2++2e-;海水中溶解的O2在铁上得电子:O2+4e-+2H2O
Zn2++2e-;海水中溶解的O2在铁上得电子:O2+4e-+2H2O![]() 4OH-。
4OH-。
(3)金属银被空气氧化生成Ag2O(黑色):4Ag+O2![]() 2Ag2O。
2Ag2O。
(4)形成Fe-Ag原电池,Fe比Ag活泼,加速腐蚀:Fe![]() Fe2++2e-,O2+4e-+2H2O
Fe2++2e-,O2+4e-+2H2O![]() 4OH-; Fe2++2OH-
4OH-; Fe2++2OH-![]() Fe(OH)2,4Fe(OH)2+O2+2H2O
Fe(OH)2,4Fe(OH)2+O2+2H2O![]() 4Fe(OH)3;2Fe(OH)3
4Fe(OH)3;2Fe(OH)3![]() Fe2O3+3H2O。
Fe2O3+3H2O。
答案:(1)潮湿土壤里的铁管形成原电池加速腐蚀。
(2)与海水形成Zn-Fe原电池,Fe是正极被保护。
(3)银被空气氧化为氧化银。
(4)在潮湿空气或水中形成Fe-Ag原电池,Fe是负极,被腐蚀。

练习册系列答案
相关题目
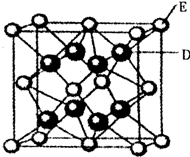 已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和.
已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和.