题目内容
7.下列实验操作、现象与结论对应关系正确的是( )| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将1g碳酸钠固体和1g碳酸氢钠固体分别加入两支试管,加10mL水溶解后,滴加1~2滴酚酞溶液 | 碳酸钠溶液显红色,碳酸氢钠溶液显浅红色 | 碳酸钠溶液碱性比碳酸氢钠溶液碱性强 |
| B | 除锈的铁钉在浓硝酸中浸泡后,用蒸馏水洗净,再加入CuSO4溶液中 | 无明显现象 | 铁不与CuSO4溶液反应 |
| C | 将SO2和CO2气体分别通入水中至饱和,立即用pH计测两溶液的pH | 前者的pH小于后者 | H2SO3酸性强于H2CO3 |
| D | 向2mL0.1mol/LNa2S溶液中滴入几滴0.1mol/LZnSO4溶液,再加入几滴0.1mol/LCuSO4溶液 | 开始有白色沉淀生成,后又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
| A. | A | B. | B | C. | C | D. | D |
分析 A.相同浓度时,碳酸钠的水解程度大;
B.常温下Fe遇浓硝酸发生钝化;
C.饱和溶液的浓度不同,应测定等浓度溶液的pH比较酸性;
D.由操作和现象可知发生沉淀的生成.
解答 解:A.相同浓度时,碳酸钠的水解程度大,由现象可知碳酸钠溶液碱性比碳酸氢钠溶液碱性强,故A正确;
B.常温下Fe遇浓硝酸发生钝化,与硫酸铜溶液不反应液,但Fe可与硫酸铜反应,故B错误;
C.饱和溶液的浓度不同,应测定等浓度溶液的pH比较酸性,操作和现象不能说明结论,故C错误;
D.Na2S溶液过量,由操作和现象可知为沉淀的生成,则不能比较ZnS、CuS溶度积(Ksp),故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握溶解度与浓度的关系、物质的性质、沉淀转化为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度中等.

练习册系列答案
相关题目
17.下列说法不正确的是( )
| A. | 多糖和蛋白质都是高分子化合物 | |
| B. | 淀粉和纤维素分子式相同、结构不同,二者互为同分异构体 | |
| C. | 蛋白质和多糖在一定条件下都能发生水解反应 | |
| D. | 蛋白质具有酸碱两性 |
18.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol甲醇中含有的共价键数为4 NA | |
| B. | 5.6g乙烯和环丁烷(C4H8)的混合气体中含的碳原子数为0.4 NA | |
| C. | 常温下,pH=2的盐酸溶液中含有的H+数目为0.02NA | |
| D. | 常温下,1L 0.5 mol/L的FeCl3溶液中,所含Fe3+数为0.5NA |
15.下列关于有机化合物的认识正确的是( )
①在铁粉存在下,苯与液溴的反应属于取代反应
②氯乙烷与NaOH水溶液共热可生成乙烯
③甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同
④苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
⑤用酸性高锰酸钾溶液可区分己烷和3-己烯
⑥用水可区分苯和溴苯.
①在铁粉存在下,苯与液溴的反应属于取代反应
②氯乙烷与NaOH水溶液共热可生成乙烯
③甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同
④苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
⑤用酸性高锰酸钾溶液可区分己烷和3-己烯
⑥用水可区分苯和溴苯.
| A. | ①②④⑤⑥ | B. | ①②③④⑤ | C. | ①③④⑤⑥ | D. | ②③④⑤⑥ |
1.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如下:
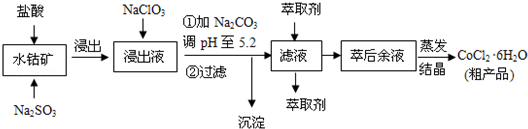
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110-120℃时,失去结晶生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+,防止Co2+转化为Co(OH)2沉淀.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+,防止Co2+转化为Co(OH)2沉淀.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
6.对于N2+3H2$?_{高温高压}^{催化剂}$2NH3,下列不同物质表示的反应速率最大的是( )
| A. | V(N2)=0.01mol•L-1•min-1 | B. | V(H2)=0.06mol•L-1•min-1 | ||
| C. | V(NH3)=0.02mol•L-1•min-1 | D. | V(H2)=0.002mol•L-1•min-1 |
 )可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等.以下是屈昔多巴的一种合成路线(通常
)可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等.以下是屈昔多巴的一种合成路线(通常 简写为BnCl,
简写为BnCl, 简写为CbzCl ):
简写为CbzCl ):
 显碱性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:
显碱性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:
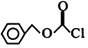 的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有6种,其中核磁共振氢谱为四组峰的结构简式为
的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有6种,其中核磁共振氢谱为四组峰的结构简式为 (任写一种).
(任写一种). .
.